
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源:2016-2017学年浙江省高一上10月月考化学试卷(解析版) 题型:填空题
有下列物质:①NaOH溶液②铜丝③液态HCl④盐酸⑤Na2SO3固体⑥CO2⑦酒精⑧葡萄糖⑨氧化钠⑩熔融氯化钠
(1)上述物质中,可导电的是 。
(2)上述物质中,属于非电解质的是 。
(3)上述状态下,属于电解质但不导电的是 。
(4)写出Na2SO3的电离方程式: 。
查看答案和解析>>
科目:高中化学 来源:2016-2017学年浙江省高一上10月月考化学试卷(解析版) 题型:选择题
下列有关胶体的说法中,不正确的是
A.胶体、溶液、浊液的分类依据是分散质微粒直径大小
B.“卤水点豆腐”、“黄河入海口处的沙洲”都与胶体的聚沉有关
C.向 1 mol•L﹣1 氯化铁溶液中加入少量的 NaOH 溶液 制取氢氧化铁胶体
制取氢氧化铁胶体
D.可以用丁达尔现象区别硫酸铜溶液和氢氧化铁胶体
查看答案和解析>>
科目:高中化学 来源:2016-2017学年西藏拉萨中学高二上第一次月考化学试卷(解析版) 题型:填空题
A.已知下列热化学方程式:
①CH3COOH(l)+2O2(g)=2CO2(g)+2H2O(l) ΔH1=-870.3 kJ/mol
②C(s)+O2(g)= CO2(g) ΔH2=-393.5 kJ/mol
③H2(g)+1/2O2(g)=H2O(l) ΔH3=-285.8 kJ/mol
则反应④2C(s)+2H2(g)+O2(g)=CH3COOH(l)的焓变为
b .①H2(g)+1/2O2(g)=H2O(l) ΔH=-285.8 kJ/mol
.①H2(g)+1/2O2(g)=H2O(l) ΔH=-285.8 kJ/mol
②H2(g)+1/2O2(g)=H2O(g) ΔH=-241.8 kJ/mol
③C(s)+1/2O2(g)=CO(g) ΔH=-110.5 kJ/mol
④C(s)+O2(g)=CO2(g) ΔH=-393.5 kJ/mol
回答下列问题:
(1)上述反应中属于放热反应的是 。
(2)H2的燃烧热为 ,C的燃烧热为 。
(3)CO的燃烧热为 ,其热化学方程式为 。
查看答案和解析>>
科目:高中化学 来源:2016-2017学年西藏拉萨中学高二上第一次月考化学试卷(解析版) 题型:选择题
在一定的条件下,CO与CH4燃烧的热化学方程式分别为
2CO(g)+O2(g)=2CO2(g)△H=-566kJ/mol
CH4(g)+2O2(g)=CO2(g)+2H2O(l)△H=-890kJ/m ol
ol
由1molCO和3molCH4组成的混和气在上述条件下完全燃烧时,释放的热量为
A.2953kJ B.2912kJ C.3236kJ D.3867kJ
查看答案和解析>>
科目:高中化学 来源:2016-2017学年天津市高一上9月调研化学试卷(解析版) 题型:实验题
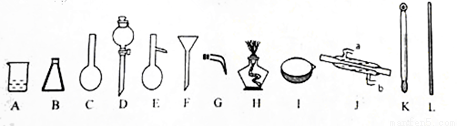
(1)填写以下仪器的名称:B D E
(2)用四氯化碳提取出溴水中Br2的方法是: ,将Br2的四氯化碳溶液和水分离开的操作是:
(3)已知Br2的沸点是58.5℃,四氯化碳沸点是78℃。将Br2的四氯化碳溶液中的Br2分离出来的操作是 。该操作需要用到的玻璃仪器有(填字母) 。
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
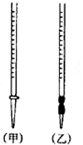 用中和滴定法测定某烧碱样品的纯度.有以下步骤:
用中和滴定法测定某烧碱样品的纯度.有以下步骤:| 测定序号 | 待测溶液的体积(mL) | 所耗盐酸标准液的体积(mL) | |
| 滴定前读数 | 滴定后读数 | ||
| 1 | 20.00 | 0.50 | 20.78 |
| 2 | 20.00 | 1.20 | 21.32 |
| 3 | 20.00 | 0.40 | 21.20 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com