
【题目】2019年3月8日,联合国妇女署在推特上发布了一张中国女科学家屠呦呦的照片。致敬她从传统中医药中找到了治疗疟疾的药物----青蒿素。
已知:青蒿素是烃的含氧衍生物,为无色针状晶体。乙醚沸点为35℃。
(1)我国提取中草药有效成分的常用溶剂有:水;或亲水性溶剂(如乙醇,与水互溶);或亲脂性溶剂(如乙醚,与水不互溶)。诺贝尔奖获得者屠呦呦及其团队在提取青蒿素治疗疟疾过程中,记录如下:“青蒿素的水煎剂无效;乙醇提取物的效用为30%~40%;乙醚提取物的效用为95%”。下列推测不合理的是_____;
A | 青蒿素在水中的溶解度很大 | B | 青蒿素含有亲脂的官能团 |
C | 在低温下提取青蒿素,效果会更好 | D | 乙二醇提取青蒿素的能力强于乙醚 |
(2)用下列实验装置测定青蒿素实验式的方法如下:
将28.2g青蒿素样品放在硬质玻璃管C中,缓缓通入空气数分钟后,再充分燃烧,精确测定装置E和F实验前后的质量,根据所测数据计算。
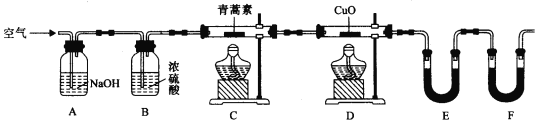
①装置D的作用是______,装置E中吸收的物质是______,装置F中盛放的物质是______。
②实验装置可能会产生误差,造成测定含氧量偏低,改进方法是______。
③合理改进后的装置进行实验,称得:
装置 | 实验前/g | 实验后/g |
E | 22.6 | 42.4 |
F | 80.2 | 146.2 |
则测得青蒿素的实验式是_____。
【答案】AD 将可能生成的CO氧化为CO2 H2O(水蒸气) 碱石灰 在装置F后连接一个防止空气中的CO2和水蒸气进入F的装置 C15H22O5
【解析】
(1)青蒿素的水煎剂无效;乙醇提取物的效用为30%~40%;乙醚提取物的效用为95%,可说明青蒿素在水中的溶解度很小,易溶于乙醚,以此解答该题;
(2)为了能准确测量青蒿素燃烧生成的CO2和H2O,实验前应通入除去了CO2和H2O的空气,并排除装置内的空气,防止干扰实验。装置D将可能生成的CO氧化为CO2,减小实验误差,装置E和F一个吸收生成的H2O,一个吸收生成的CO2,应先吸水后再吸收CO2,据此分析解答。
(1) A.由题给信息可知青蒿素在水中的溶解度很小,故A错误;
B.青蒿素易溶于乙醚,而乙醚为亲脂性溶剂,可说明青蒿素含有亲脂的官能团,故B正确;
C.因乙醚的沸点较低,则在低温下提取青蒿素,效果会更好,故C正确;
D.乙醇提取物的效用为30%~40%;乙醚提取物的效用为95%,乙二醇与乙醇类似,属于亲水性溶剂,提取青蒿素的能力弱乙醚,故D错误;
答案选AD;
(2)为了能准确测量青蒿素燃烧生成的CO2和H2O,实验前应通入除去了CO2和H2O的空气,并排除装置内的空气,防止干扰实验。装置D将可能生成的CO氧化为CO2,减小实验误差,E和F一个吸收生成的H2O,一个吸收生成的CO2,应先吸水后再吸收CO2,所以装置E内装CaCl2或P2O5,装置F内装碱石灰,而在F后应再加入一个装置防止外界空气中CO2和H2O进入的装置。
①根据上面的分析可知,装置E中盛放的物质是CaCl2或P2O5,吸收水蒸气,装置F中盛放的物质是碱石灰是吸收二氧化碳,装置D可以将生成的CO转化成CO2而被吸收,
故答案为:将可能生成的CO氧化为CO2;H2O(水蒸气);碱石灰;
②该实验装置可能会产生误差,造成测定含氧量偏低,改进方法是在装置F后连接一个防止空气中的CO和水蒸气进入F的装置,故答案为:在装置F后连接一个防止空气中的CO和水蒸气进入F的装置;
③由数据可知m(H2O)=42.4-22.6=19.8g,所以n(H2O)=![]() =1.1mol;m(CO2)=146.2-80.2=66g,所以n(CO2)=
=1.1mol;m(CO2)=146.2-80.2=66g,所以n(CO2)=![]() =1.5mol,所以青蒿素中氧原子的质量为m(O)=28.2g-(1.1mol×2×1g/mol)-(1.5 mol×12 g/mol)=8g,所以n(O)=
=1.5mol,所以青蒿素中氧原子的质量为m(O)=28.2g-(1.1mol×2×1g/mol)-(1.5 mol×12 g/mol)=8g,所以n(O)=![]() =0.5mol,N(C)∶N(H)∶N(O)=1.5∶2.2∶0.5=15∶22∶5,所以C15H22O5,故答案为:C15H22O5。
=0.5mol,N(C)∶N(H)∶N(O)=1.5∶2.2∶0.5=15∶22∶5,所以C15H22O5,故答案为:C15H22O5。


科目:高中化学 来源: 题型:
【题目】写出下列有机物的系统命名或结构简式:
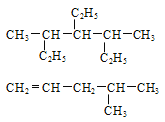
(1)_____________
(2)_____________
(3)4,4,5-三甲基-2-己炔 _______________
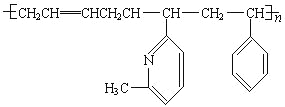
(4)新型弹性材料“丁苯吡橡胶”的结构简式如下:其单体为______________(有几种写几种)
(5)如下表所示,为提纯下列物质(括号内为少量杂质),填写所选用的除杂试剂与主要分离方法
不纯物质 | 除杂试剂 | 分离方法 | |
1 | 溴苯(Br2) | __________ | __________ |
2 | 乙醛(乙酸) | __________ | __________ |
3 | 乙酸乙酯(乙酸) | __________ | __________ |
4 | 乙醇(苯酚) | __________ | __________ |
5 | 硝基苯(硝酸) | __________ | __________ |
(6)①C5H12O的醇,在一定条件下能发生催化氧化反应,产物能与新制的氢氧化铜反应生成红色沉淀,醇的核磁共振氢谱中有三组峰,写出满足上述条件的醇的结构简式______
②C5H12O的醇,在一定条件下不能发生消去反应,写出满足条件的醇的结构简式______
③分子式为C5H12O,不能与金属钠反应.核磁共振氢谱中有四组峰,峰的面积比为3:2:1:6,写出满足上述条件的物质的结构简式______.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】CH4是一种清洁、高效、具有优良的环保性能的燃料,其燃烧热为890.3KJ·mol-1。它可以作为燃料电池的燃料。
(1)写出甲烷燃烧的热化学方程式:________;
(2)已知H2(g)和C(S)的燃烧热分别是285.8kJ·mol-1、393.5kJ·mol-1;则反应C(S)+ 2H2(g)=CH4(g)的反应热⊿H=______________;
(3)以甲烷、空气、氢氧化钾溶液为原料,惰性电极为电极可以构成燃料电池。该电池的负极反应式为:___________________;
(4)用(3)中的燃料电池为电源,以石墨为电极电解500mL滴有酚酞的NaCl溶液,装置如图所示:
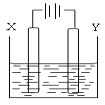
①请写出电解过程中阴极附近观察到的现象:___________________。
②到燃料电池消耗2.8LO2(标准状况下)时,计算此时NaCl溶液的pH=____(假设溶液的体积不变,气体全部从溶液中逸出)。
在Y极通过的电子的物质的量为:______________。
③电解之后,要使溶液恢复原状,应该向溶液中加入物质_____(填名称),溶液中Cl―流向___极(填“X”或“Y”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】取50.0mLNa2CO3和Na2SO4的混合溶液,加入过量BaCl2溶液后得到14.51g白色沉淀,用 过量稀硝酸处理后沉淀量减少到4.66g,并有气体放出。试计算:
(1)原混合溶液中Na2CO3和Na2SO4的物质的量浓度_______________;
(2)产生的气体在标准状况下的体积_____________。(要有过程)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】镇咳药沐舒坦可由化合物甲和化合物乙在一定条件下制得:

下列有关叙述正确的是( )
A. 甲的分子式为C7H4NBr2Cl
B. 沐舒坦分子中最多有13个碳原子共平面
C. 乙遇FeCl3溶液显紫色
D. 反应过程中加入适量K2CO3可提高沐舒坦的产率
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】次磷酸(H3PO2)是一种精细磷化工产品,具有较强还原性,回答下列问题:
(1)H3PO2是一元中强酸,写出其电离方程式:_____________________________。
(2)H3PO2及NaH2PO2均可将溶液中的Ag+还原为银,从而可用于化学镀银。
①H3PO2 中,P元素的化合价为________。
②利用H3PO2进行化学镀银反应中,氧化剂与还原剂的物质的量之比为4∶1,则氧化产物为________(填化学式)。
③NaH2PO2 为________(填“正盐”或“酸式盐”),其溶液显 ________(填“弱酸性”、“中性”或“弱碱性”)。
(3)H3PO2的工业制法是:将白磷(P4)与Ba(OH)2溶液反应生成PH3气体和Ba(H2PO2)2,后者再与H2SO4反应。写出白磷与Ba(OH)2溶液反应的化学方程式:__________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】乙酸苯甲酯对花香和果香的香气有提升作用,故常用于化妆品工业和食品工业。乙酸苯甲酯可以用下面的设计方案合成。
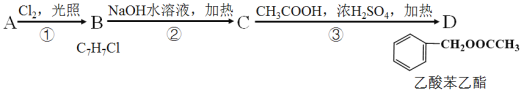
(1)A的结构简式为_________________;B的官能团名称为_______________________;
(2)反应②的化学方程式为____________________________________________________;
(3)D有很多同分异构体,苯环上只有一个取代基且属于酯类化合物的同分异构体共5个,已知其中3个的结构简式是:
![]()
![]()
![]()
请写出另外两个同分异构体的结构简式__________________、____________________;
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某溶液中可能含有如下离子:H+、Mg2+、Al3+、NH4+、Cl-、AlO2-。当向该溶液中逐滴加入NaOH溶液时,产生沉淀的物质的量(n)与加入NaOH溶液的体积(V)的关系如图所示,下列说法正确的是( )

A. 原溶液中一定含有的阳离子是H+、Mg2+、Al3+、NH4+
B. 反应最后形成的溶液中的溶质含AlCl3
C. 原溶液中Al3+与NH的物质的量之比为1∶3
D. 原溶液中含有的阴离子是Cl-、AlO2-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下表中评价合理的是
选项 | 化学反应及其离子方程式 | 评 价 |
A | NaHSO4溶液与Ba(OH)2溶液反应至 SO42-沉淀完全: 2H++SO42-+Ba2++2OH- = BaSO4↓ + 2H2O | 正 确 |
B | 向碳酸镁溶液中加入足量稀盐酸: CO32-+2H+=CO2↑+H2O | 错误,碳酸镁不应写成离子形式 |
C | 向沸水中滴加饱和的氯化铁溶液至液体变为红褐色: Fe3++3H2O = Fe(OH)3↓+3H+ | 正 确 |
D | NaOH溶液中通入少量CO2反应:OH-+CO2=HCO3- | 正 确 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com