下列说法正确的是( )
A.Na2O2和C18O2反应的产物碳酸钠,它的相对分子质量为110
B.1molAl和足量的NaOH溶液充分反应时,同时有1molH2O参加
C.反应Cu+H2SO4→CuSO4+H2↑,在一定条件下也能实现
D.常见自来水的杀菌消毒剂有:Cl2、Ca(ClO)2、ClO2、Na2FeO4等,效果最好的是Cl2
【答案】
分析:A、根据CO
2和Na
2O
2反应的本质可知生成Na
2C
18O
2O;
B、根据Al和NaOH溶液反应的本质来分析;
C、根据电解原理;
D、根据相同质量的消毒剂得到电子的多少来比较.
解答:解:A、Na
2O
2和CO
2发生反应:2Na
2O
2+2CO
2═2Na
2CO
3+O
2 反应的本质是Na
2O
2遇CO
2后Na
2O
2中每两个氧原子中的一个将转变为气体逸出,CO
2中的2个氧进入碳酸钠,碳酸钠中有2个
18O,它的相对分子质量:23×2+12+16+18×2=110,故A正确;
B、Al和NaOH溶液反应的本质是铝先和水反应生成氢氧化铝:2Al+6H
2O=2Al(OH)
3+3H
2↑,然后氢氧化铝再和NaOH反应:Al(OH)
3+NaOH=NaAlO
2+2H
2O,所以 1molAl和足量的NaOH溶液充分反应时,同时有3molH
2O参加,同时生成2molH
2O,故B错误;
C、由于Cu的还原性比H
2弱,所以,在通常情况下,Cu不和稀硫酸发生反应,但要使该反应Cu+H
2SO
4=CuSO
4+H
2↑发生,只能采用电解法,阳极是Cu,阳极:Cu-2e═Cu
2+,阴极导电材料任选,阴极:2H
++2e═H
2↑,电解质溶液必须是H
2SO
4,故C正确;
D、设Cl
2、Ca(ClO)
2、ClO
2、Na
2FeO
4的质量均为1 g,则被还原时,它们得到电子的物质的量分别为:
Cl
2:
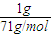
×2=0.028 mol,Ca(ClO)
2:
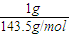
×4=0.027 mol,
ClO
2:
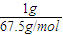
×5=0.074 mol,Na
2FeO
4:
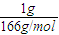
×3=0.018 mol,
得到电子越多,消毒效率越大,所以四种物质的消毒效率由大到小的顺序是ClO
2>Cl
2>Ca(ClO)
2>Na
2FeO
4,故D错误;
故选AC.
点评:本题主要考查了化学反应的本质、电解原理的应用、消毒效率大小的比较,这些知识点难度较大,学生做起来比较吃力.

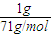 ×2=0.028 mol,Ca(ClO)2:
×2=0.028 mol,Ca(ClO)2: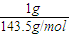 ×4=0.027 mol,
×4=0.027 mol,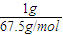 ×5=0.074 mol,Na2FeO4:
×5=0.074 mol,Na2FeO4: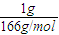 ×3=0.018 mol,
×3=0.018 mol,


 Sn(s,白)△H3=+2.1kJ?mol-1,
Sn(s,白)△H3=+2.1kJ?mol-1,