
| A. | ①③⑤ | B. | ②③⑤ | C. | ①②④ | D. | ②④ |
分析 ①化石燃料属于不可再生资源,且化石燃料的使用会产生污染物;
②研发易降解的生物农药,能降低农药残留;
③应用高效洁净的能源转换技术,提高能源利用率;
④田间焚烧秸秆,不完全燃烧产生可吸收颗粒物,同时增加二氧化碳排放;
⑤推广使用节能环保材料,节约资源、保护环境.
解答 解:①化石燃料燃烧会产生可吸收颗粒物、二氧化硫等污染物,化石燃料属于不可再生资源,加快化石燃料的开采与使用会增加污染物的排放量,故不符合题意;
②研发易降解的生物农药能减少生物药物残留,减少污染物的排放,故符合题意;
③应用高效洁净的能源转换技术,可以节约能源,减少二氧化碳的排放,故符合题意;
④田间焚烧秸秆,秸秆不完全燃烧产生固体颗粒物,同时增加二氧化碳的排放,故不符合题意;
⑤推广使用节能环保材料可以节约能源,减少二氧化碳的排放,故符合题意.
即有利于节能减排、保护环境的是②③⑤,
故选B.
点评 本题考查环境保护问题,学生应明确习题中含有当前的社会热点是高考的一大特点,学生应学会把社会热点和课本知识点联系起来来解答即可,突出了化学的实用性,平时要注意积累,题目难度不大.


 优秀生应用题卡口算天天练系列答案
优秀生应用题卡口算天天练系列答案 浙江之星课时优化作业系列答案
浙江之星课时优化作业系列答案科目:高中化学 来源: 题型:解答题
 .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
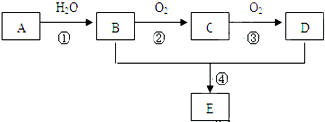
 是重要的化工原料,其合成过程如图:
是重要的化工原料,其合成过程如图:
 .
.查看答案和解析>>
科目:高中化学 来源: 题型:实验题

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 向Fe(NO3)2稀溶液中加入稀盐酸:Fe2++2H++NO3-═Fe3++NO2↑+H2O | |
| B. | 向(NH4)2Mg(SO4)2溶液中加入少量的Na2O:Mg2++Na2O+H2O═Mg(OH)2↓+2Na+ | |
| C. | 向Fe(NO3)3溶液中加入过量的HI溶液:2Fe3++2I-═2Fe2++I2 | |
| D. | 向漂白粉溶液中通入SO2:Ca2++ClO-+SO2+H2O═CaSO3↓+2HClO |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①②③ | B. | ①②④⑤ | C. | ①②③④ | D. | ②④ |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
 ,它配以辅料丙二醇溶成针剂用于临1,3,5
,它配以辅料丙二醇溶成针剂用于临1,3,5查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com