
| »ıÀ·ªØ—ß Ω | CH3COOH | HCN | H2CO3 |
| µÁ¿Î∆Ω∫‚≥£ ˝£®25°Ê£© | 1.8°¡10£≠5 | 4.9°¡10£≠10 | K1=4.3°¡10£≠7 K2=5.6°¡10£≠11 |



| ƒÍº∂ | ∏þ÷–øŒ≥à | ƒÍº∂ | ≥ı÷–øŒ≥à |
| ∏þ“ª | ∏þ“ª√‚∑—øŒ≥ÃÕ∆ºˆ£° | ≥ı“ª | ≥ı“ª√‚∑—øŒ≥ÃÕ∆ºˆ£° |
| ∏þ∂˛ | ∏þ∂˛√‚∑—øŒ≥ÃÕ∆ºˆ£° | ≥ı∂˛ | ≥ı∂˛√‚∑—øŒ≥ÃÕ∆ºˆ£° |
| ∏þ»˝ | ∏þ»˝√‚∑—øŒ≥ÃÕ∆ºˆ£° | ≥ı»˝ | ≥ı»˝√‚∑—øŒ≥ÃÕ∆ºˆ£° |
ø∆ƒø£∫∏þ÷–ªØ—ß ¿¥‘¥£∫≤ªœÍ –գ∫µ•—°Ã‚
| A£Æ1.0 mol°§L£≠1µƒKNO3»Ð“∫£∫H£´°¢Fe2£´°¢Cl£≠°¢SO42£≠ |
| B£Æ±•∫Õ¬»ÀÆ÷–£∫NH4£´°¢SO32£≠°¢AlO2£≠°¢Cl£≠ |
| C£Æ”ά¡∑¥”¶≤˙…˙¥Û¡ø«‚∆¯µƒ»Ð“∫£∫Na£´°¢K£´°¢CO32£≠°¢NO3£≠ |
| D£Æc(H£´)=1.0°¡10£≠13mol/L»Ð“∫÷–£∫K£´°¢Na£´°¢CH3COO£≠°¢Br£≠ |
≤Èø¥¥∞∏∫ÕΩ‚Œˆ>>
ø∆ƒø£∫∏þ÷–ªØ—ß ¿¥‘¥£∫≤ªœÍ –գ∫ÃÓø’Â
 £¨µÁΩ‚÷ Õ®π˝±√‘⁄¥¢πÞ∫ÕµÁ≥ÿº‰—≠ª∑£ª¿Î◊”—°‘Ò–‘ƒ§÷ª‘ –̃∆¿Î◊”Õ®π˝°£
£¨µÁΩ‚÷ Õ®π˝±√‘⁄¥¢πÞ∫ÕµÁ≥ÿº‰—≠ª∑£ª¿Î◊”—°‘Ò–‘ƒ§÷ª‘ –̃∆¿Î◊”Õ®π˝°£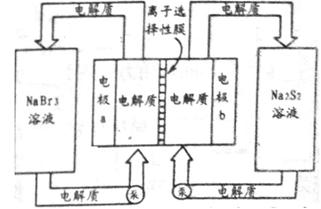
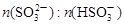 πÿœµ»Áœ¬±Ì£∫
πÿœµ»Áœ¬±Ì£∫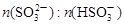 | 91°√9 | 1°√1 | 9°√91 |
| pH£®25°Ê£© | 8.2 | 7.2 | 6.2 |
≤Èø¥¥∞∏∫ÕΩ‚Œˆ>>
ø∆ƒø£∫∏þ÷–ªØ—ß ¿¥‘¥£∫≤ªœÍ –գ∫µ•—°Ã‚
| ±ý∫≈ | HX | YOH | »Ð“∫ê˝ | ¡£◊”≈®∂» |
| ¢Ÿ | «øÀ· | «øºÓ | V(HX)=" V" (YOH) | c(HX) + c(X£≠) = c(Y+) |
| ¢⁄ | »ıÀ· | »ıºÓ | V(HX)£ºV(YOH) | c(X£≠) £º c(Y+) |
| ¢€ | «øÀ· | «øºÓ | V(HX)= V(YOH) | c(H+)£æc(YOH) + c(OH£≠) |
| ¢Ð | »ıÀ· | »ıºÓ | V(HX)£æV(YOH) | c(Y+) + c(H+) = c(X£≠) + c(OH£≠) |
≤Èø¥¥∞∏∫ÕΩ‚Œˆ>>
ø∆ƒø£∫∏þ÷–ªØ—ß ¿¥‘¥£∫≤ªœÍ –գ∫µ•—°Ã‚
| A£ÆK+°¢Cl-°¢Na+°¢SO32- | B£ÆBa2+°¢NO3-°¢Al3+°¢Br- |
| C£ÆK+°¢NH4+°¢I-°¢CO32- | D£ÆNa+°¢Cu2+°¢NH3°§H2O°¢SO42- |
≤Èø¥¥∞∏∫ÕΩ‚Œˆ>>
ø∆ƒø£∫∏þ÷–ªØ—ß ¿¥‘¥£∫≤ªœÍ –գ∫µ•—°Ã‚
| A£ÆBa2+°¢Cl£≠°¢SO42£≠°¢K+ | B£ÆMg2+°¢SO42£≠°¢Na+°¢Cl£≠ |
| C£ÆH+°¢CO32£≠°¢Al3+°¢Cl£≠ | D£ÆK+°¢Fe2+°¢NO3£≠°¢H+ |
≤Èø¥¥∞∏∫ÕΩ‚Œˆ>>
ø∆ƒø£∫∏þ÷–ªØ—ß ¿¥‘¥£∫≤ªœÍ –գ∫µ•—°Ã‚
| A£ÆFe3+°¢Na+°¢SO42£≠°¢Cl£≠ |
| B£ÆH+°¢Fe2+°¢Cl£≠°¢NO3£≠ |
| C£ÆAg+°¢Na+°¢CO32£≠°¢NO3£≠ |
| D£ÆAl3+°¢K+°¢Cl£≠°¢AlO2£≠ |
≤Èø¥¥∞∏∫ÕΩ‚Œˆ>>
ø∆ƒø£∫∏þ÷–ªØ—ß ¿¥‘¥£∫≤ªœÍ –գ∫µ•—°Ã‚
A£ÆŒÔ÷ µƒ¡ø≈®∂»œýµ»µƒCH3COOH∫ÕCH3COONa»Ð“∫µ»Ãª˝ªÏ∫œ£∫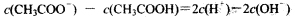 |
B£ÆNa2CO3»Ð“∫÷–£¨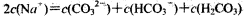 |
C£ÆpHœýµ»µƒCH3COONa°¢NaClO°¢NaHCO3»˝÷÷»Ð“∫£∫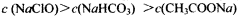 |
D£ÆNH4Cl»Ð“∫∫ÕNaOH»Ð“∫ªÏ∫œÀ˘µ√µƒ÷––‘»Ð“∫÷–£∫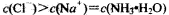 |
≤Èø¥¥∞∏∫ÕΩ‚Œˆ>>
ø∆ƒø£∫∏þ÷–ªØ—ß ¿¥‘¥£∫≤ªœÍ –գ∫µ•—°Ã‚
A£Æ‘⁄c(H+)=10-10 mol/Lµƒ»Ð“∫÷– Al3+°¢NH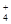 °¢Cl£≠ °¢NO °¢Cl£≠ °¢NO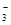 |
B£ÆpH÷µŒ™1µƒ»Ð“∫ Fe2+°¢Na+ °¢SO42-°¢NO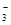 |
| C£ÆÀƵÁ¿Î≥ˆ¿¥µƒc(H+)=10£≠12mol/Lµƒ»Ð“∫ K+°¢HCO3-°¢Cl£≠°¢ClO- |
D£ÆpH÷µŒ™13µƒ»Ð“∫ K+°¢CO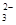 °¢Na+°¢[Al(OH)]4£≠ °¢Na+°¢[Al(OH)]4£≠ |
≤Èø¥¥∞∏∫ÕΩ‚Œˆ>>
π˙º —ß–£”≈—° - ¡∑œ∞≤·¡–±Ì - ‘¡–±Ì
∫˛±± °ª•¡™Õ¯Œ•∑®∫Õ≤ª¡º–≈œ¢æŸ±®∆Ωî | Õ¯…œ”–∫¶–≈œ¢æŸ±®◊®«¯ | µÁ–≈’©∆≠柱®◊®«¯ | …Ê¿˙ ∑–ÈŒÞ÷˜“”–∫¶–≈œ¢æŸ±®◊®«¯ | …Ê∆Û«÷»®æŸ±®◊®«¯
Œ•∑®∫Õ≤ª¡º–≈œ¢æŸ±®µÁª∞£∫027-86699610 柱®” œ‰£∫58377363@163.com