

 期末冲刺100分创新金卷完全试卷系列答案
期末冲刺100分创新金卷完全试卷系列答案科目:高中化学 来源:不详 题型:单选题
| A.③④ | B.①②③④ | C.①③④ | D.全部 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题

查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.金、银、铜、铁、钠五种金属元素中,只有钠属于主族元素 |
| B.元素周期表中的所有副族元素都是金属元素,副族包含过渡元素和Ⅷ族 |
| C.元素周期表第8、9、10三列合称Ⅷ族,Ⅷ族是元素周期表所有族中元素种类最多的族 |
| D.O、S、Na、K的原子半径依次增大;KOH、Mg(OH)2、Al(OH)3的碱性逐渐增强 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
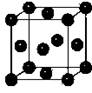
| 元素 | 性质或结构信息 |
| X | 单质为双原子分子,分子中含有3对共用电子对,常温下单质气体性质稳定,但其原子较活泼。 |
| Y | 二价阳离子的外围电子层排布为3d9 |
| T | 原子核外s轨道电子总数等于p轨道电子总数;人体内含量最多的元素,且其单质是常见的助燃剂。 |
| Q | 第三周期主族元素中原子半径最小。 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
 。
。 为Y。在等体积、等pH的X、Y的溶液中分别加入等质量的锌粉,反应后若最后仅有一份溶液中存在锌粉,则反应过程中两溶液中反应速率的大小关系是:X Y(填“>”、“=”或“<”)
为Y。在等体积、等pH的X、Y的溶液中分别加入等质量的锌粉,反应后若最后仅有一份溶液中存在锌粉,则反应过程中两溶液中反应速率的大小关系是:X Y(填“>”、“=”或“<”)查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com