
| A. | 玻璃 | B. | 纤维素 | C. | 天然油脂 | D. | 冰水混合物 |
科目:高中化学 来源: 题型:解答题
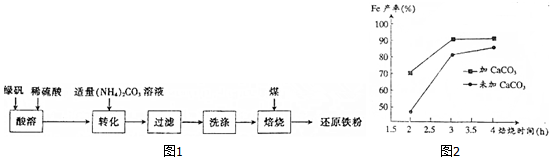
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 向氯化铁溶液中加入Cu单质:Cu+Fe3+═Fe2++Cu2+ | |
| B. | 向盐酸中加入Cu:Cu+2H+═Cu2++H2↑ | |
| C. | 向NaOH溶液中加入硫酸:OH-+H+═H2O | |
| D. | 向CuSO4溶液中加入钠:2Na+Cu2+═2Na++Cu |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

| Fe3 | Fe2+ | Cu2+ | Al3+ | |
| 开始沉淀时的 pH | 2.2 | 7.5 | 5.2 | 3.7 |
| 完全沉淀时的 pH | 3.2 | 9.0 | 6.7 | 4.7 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1 g H2和8 g O2 | |
| B. | 常温常压下,28 g CO和6.02×1022个CO分子 | |
| C. | 0.1 mol HCl和2.24 L He | |
| D. | 150℃、1.01×105 Pa时,18 L H2O和18 L CO2 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
 如右图所示的两个实验装置中,溶液的体积均为200mL,开始时电解质溶液的浓度均为0.1mol/L,工作一段时间后,测得导线中均通过0.01mol电子,若不考虑盐的水解和溶液体积的变化,则下列叙述中正确的是( )
如右图所示的两个实验装置中,溶液的体积均为200mL,开始时电解质溶液的浓度均为0.1mol/L,工作一段时间后,测得导线中均通过0.01mol电子,若不考虑盐的水解和溶液体积的变化,则下列叙述中正确的是( )| A. | 右边电极上生成物质的质量:①=② | |
| B. | 两级上产生气体的体积:①<② | |
| C. | 溶液的pH变化:①增大,②不变 | |
| D. | 电极反应式:①中阳极2H2O-4e-=4H++O2↑②中负极2H+-2e-=H2↑ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com