
对下列各项实验过程中所产生的部分现象的描述中,不正确的是
[ ]
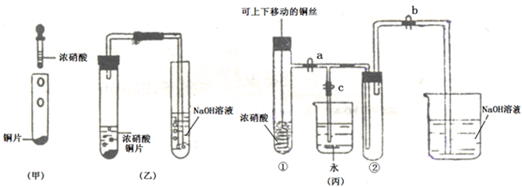
A.Cu片投入浓HNO3溶液中反应后,溶液呈蓝色
B.常温下,将铝片投入浓硝酸中,马上产生大量气体
C.灼热的木炭投入热的浓硝酸中后,能剧烈反应
D.氨气能在空气中燃烧并生成红棕色气体
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:阅读理解

查看答案和解析>>
科目:高中化学 来源: 题型:阅读理解

查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源:浙江省宁波市2010届高三三模考试(理综)化学部分 题型:实验题
(14分)油条是一种深受群众喜爱的传统食品,在百姓早餐桌上一直占有重要位置。但油条中铝含量超标问题十分普遍,是影响群众健康的食品安全隐患。从2009年5月下旬开始,浙江省的油条加工停用含铝食品的添加剂,逐步转换为无铝添加剂配方和工艺,从而保证百姓吃上安全、放心的油条。油条无铝配方由碳酸氢钠(小苏打)、碳酸氢铵(臭粉)组成。为测定试样中小苏打的质量分数w(NaHCO3),实验小组同学设计了如下装置进行实验。

|
实验过程
①按图组装仪器,检查装置的气密性;
②将试样m1g放入硬质玻璃管中,装置B、C、D中药品如图,已知加药品后装置B的质量为m2g、装置C的质量为m3g;
③关闭活塞a,点燃酒精灯加热试样,直到B装置中无气泡冒出后,打开活塞a向装置中通入N2,一段时间后,撤掉酒精灯,关闭活塞a;
④称得装置B的质量为m4g、装置C的质量为m5g。
请回答以下问题(装置中原有空气对实验的影响忽略不计):
(1)装置A中发生反应的化学方程式为 ▲ 。
(2)装置B的作用为 ▲ 。
装置C的作用为 ▲ 。
(3)实验过程中通入N2的目的为 ▲ 。
(4)用下列各项所提供的数据能计算出w(NaHCO3)的是( ▲ ) (填选项字母)
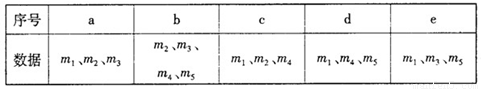
(5)实验结束后发现装置A中硬质玻璃管右端有水珠,你认为利用实验中所提供的数据还能否得到准确的w(NaHCO3) ▲ (填“能”或“不能”)。若能,则w(NaHCO3)的计算式为: ▲ ,若不能,此问不作答。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com