
氧化还原反应在生产、生活中应用广泛,酸性KMnO4、H2O2、Fe(NO3)3是重要的氧化剂.用所学知识回答问题:
(1)3H2SO4+2KMnO4+5H2O2=K2SO4+2MnSO4+5O2↑+8H2O,当有6molH2SO4参加反应的过程中,有 mol还原剂被氧化。
(2)在稀硫酸中,KMnO4能将H2C2O4氧化为CO2。该反应的化学方程式为
(3)取300mL 0.2mol/L的KI溶液与一定量的酸性KMnO4溶液恰好反应,生成等物质的量的I2和KIO3,则消耗KMnO4的物质的量的是 mol。
(4)在Fe(NO3)3溶液中加入Na2SO3溶液,溶液先由棕黄色变为浅绿色,过一会又变为棕黄色,溶液先变为浅绿色的离子方程式是 ,又变为棕黄色的原因是
 核心素养学练评系列答案
核心素养学练评系列答案 单元期中期末卷系列答案
单元期中期末卷系列答案科目:高中化学 来源:2015-2016学年河北省高二上学期第一次月考化学试卷(解析版) 题型:选择题
指常温下,1 mol化学键分解成气态原子所需要的能量用E表示。结合表中信息判断下列说法不正确的是
共价键 | H-H | F-F | H-F | H-Cl | H-I |
E(kJ·mol -1 ) | 436 | 157 | 568 | 432 | 298 |
A.432 kJ·mol -1>E(H-Br)>298 kJ·mol -1
B.表中最稳定的共价键是H—F键
C.H 2(g)→2H(g)△H=+436 kJ·mol -1
D.H2(g)+F2(g)=2HF(g)△H=—25 kJ·mol -1
查看答案和解析>>
科目:高中化学 来源:2015-2016学年吉林省高二上期中考试化学试卷(解析版) 题型:选择题
下列有关中和滴定的操作:①用标准液润洗滴定管;②往滴定管内注入标准溶液;③检查滴定管是否漏水;④滴定;⑤滴加指示剂于待测液;⑥洗涤。正确的操作顺序是
A.③⑥①②⑤④ B.⑤①②⑥④③
C.⑤④③②①⑥ D.③①②④⑤⑥
查看答案和解析>>
科目:高中化学 来源:2015-2016学年四川树德中学高一上10月阶段测化学试卷(解析版) 题型:选择题
可能由 Al、 Mg、 Cu、 Fe 中的若干金属组成的合金 2.4 克与足量的硫酸溶液反应, 产生标准状况时的氢气 2.24L,则关于合金的组成的叙述正确的是
A.一定有 Mg B.若有 Al 则一定有 Fe
C.若有 Cu 则一定有 Al D.若有 Mg 则一定有 Cu
查看答案和解析>>
科目:高中化学 来源:2015-2016学年河北省高二上第二次月考化学试卷(解析版) 题型:选择题
常温时,纯水中由水电离的c(H+)=a,pH=1的盐酸中由水电离的c(H+)=b,0.2 mol/L的盐酸与0.1 mol/L的氢氧化钠溶液等体积混合后,由水电离的c(H+)=c,则a、b、c的关系正确的是
A.a>b=c B.a>c>b C.c>b>a D.b>c>a
查看答案和解析>>
科目:高中化学 来源:2016届湖南省衡阳市高三上学期第二次月考化学试卷(解析版) 题型:实验题
(16分)通过煤的气 化和液化,使碳及其化合物得以广泛应用。
化和液化,使碳及其化合物得以广泛应用。
I.工业上先用煤转化为CO,再利用CO和水蒸气反应制H2时,存在以下平衡:
CO(g)+H2O(g) CO2(g)+H2(g)
CO2(g)+H2(g)
(1)向1L恒容密闭容器中充入CO和H2O(g),800℃时测得部分数据如下表。
t/min | 0 | 1 | 2 | 3 | 4 |
n(H2O)/mol | 0.600 | 0.520 | 0.450 | 0.350 | 0.350 |
n(CO)/mol | 0.400 | 0.320 | 0.250 | 0.150 | 0.150 |
则该温度下反应的平衡常数K= 。(保留2位有效数字)
(2)相同条件下,向2L恒容密闭容器中充入1molCO、1mol H2O(g)、2molCO2、2mo1 H2,此时v (正)_____________ v (逆)(填“>” “=” 或 “<”)。
II.已知CO(g)、H2(g)、CH3OH(l)的燃烧热分别为283 kJ·mol-1、286 kJ·mol-1、726 kJ·mol-1。
(3)利用CO、H2合成液态甲醇的热化学方程式为 。
(4)依据化学反应原理,分析增加压强对制备甲醇反应的影响 。
III.为摆脱对石油的过度依赖,科研人员将煤液化制备汽油,并设计了汽油燃料电池,电池工作原理如右图所示:一个电极通入氧气,另一电极通入汽油蒸气,电解质是掺杂了Y2O3的ZrO2晶体,它在高温下能传导O2—。
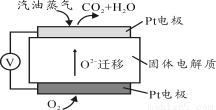
(5)以辛烷(C8H18)代表汽油,写出该电池工作时的负极反应方程式 。
(6)已知一个电子的电量是1.602×10—19C,用该电池电解饱和食盐水,当电路中通过1.929×105C的电量时,生成NaOH g。
Ⅳ.煤燃烧产生的CO2是造成温室效应的主 要气体之一。
要气体之一。
(7)将CO2转化成有机物可有效地实现碳循环。如:
a.6CO2+6H2O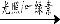 C6H12O6+6O2 b.2CO2 + 6H2
C6H12O6+6O2 b.2CO2 + 6H2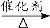 C2H5OH +3H2O
C2H5OH +3H2O
c.CO2 + CH4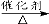 CH3COOH d.2CO2 + 6H2
CH3COOH d.2CO2 + 6H2 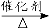 CH2=CH2 + 4H2O
CH2=CH2 + 4H2O
以上反应中,最节能的是 ,反应b中理论上原子利用率为 。
查看答案和解析>>
科目:高中化学 来源:2015-2016学年河北省高一上第一次月考化学试卷(解析版) 题型:填空题
(Ⅰ)在标准状况下,体积为8.96 L的CO和CO2的混合气体共14.4 g。
(1)CO的质量为______________g。
(2)CO的体积为______________L。
(3)混合气体的平均摩尔质量为____________g·mol-1。
(4)混合气体的密度为____________g·L-1。(小数点后保留1位)
(Ⅱ)现要配制1 mol·L-1 Na2CO3溶液250mL,求:
①需要固体Na2CO3____________g;
②需要含结晶水的碳酸钠晶体(Na2CO3·10H2O)____________g;
③需要物质的量浓度为4 mol·L-1的Na2CO3溶液____________mL;
查看答案和解析>>
科目:高中化学 来源:2015-2016学年江西省高一上第一次段考化学试卷(解析版) 题型:选择题
在150℃时碳酸铵可以受热完全分解[(NH4)2CO3 2NH3↑+H2O↑+CO2↑],则其完全分解后所产生的气态混合物的密度是相同条件下氢气密度的
2NH3↑+H2O↑+CO2↑],则其完全分解后所产生的气态混合物的密度是相同条件下氢气密度的
A.48倍 B.24倍 C.12倍 D.96倍
查看答案和解析>>
科目:高中化学 来源:2016届黑龙江省牡丹江市高三9月月考化学试卷(解析版) 题型:选择题
某学生设计了如下方法对X盐进行鉴定:

由此分析,下列结论中正确的是
A.X中一定有Fe3+ B.X一定为FeBr2溶液
C.Y为AgI沉淀 D.Z中一定有Fe3+
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com