
【题目】(1)下列反应中,属于放热反应的是________,属于吸热反应的是________(填序号)。
①煅烧石灰石 ②木炭燃烧 ③炸药爆炸 ④酸碱中和 ⑤生石灰与水作用制熟石灰 ⑥食物因氧化而腐败
(2)用铜、银与硝酸银设计一个原电池,负极的电极反应式是_______________。
(3)用锌片、铜片连接后浸入稀硫酸溶液中,构成了原电池,工作一段时间,锌片的质量减少了3.25 g,铜表面析出了氢气________L(标准状况)。
(4)现在同学们学过了取代反应、加成反应,请将下列物质发生的反应填写在下表中。
①由乙烯制1,2-二氯乙烷;②乙烷与氯气光照;③乙烯使溴的四氯化碳溶液褪色;
④乙烯通入酸性高锰酸钾溶液;⑤由苯制取溴苯;⑥乙烷在空气中燃烧;
⑦由苯制取硝基苯;⑧由苯制取环己烷
反应类型 | 取代反应 | 加成反应 |
反应 | _____ | ______ |
(5)某烃在标准状况下的密度为3.215 g/L,现取3.6 g该烃完全燃烧,将全部产物依次通入足量的浓硫酸和碱石灰,浓硫酸增重5.4 g,碱石灰增重11 g,则:
①该烃分子的摩尔质量______。
②该烃的分子式________。
③若该烃的一氯代物只有一种,则该烃的结构简式为______。
【答案】 ②③④⑤⑥ ① Cu-2e-===Cu2+ 1.12 ②⑤⑦ ①③⑧ 72 g·mol-1 C5H12 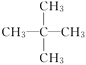
【解析】(1)①煅烧石灰石(主要成分是CaCO3)制生石灰(CaO)是分解反应,属于常见的吸热反应;②燃烧木炭取暖是物质的燃烧,放出热量,属于常见的放热反应;③炸药爆炸要放出热量,属于放热反应;④酸与碱的中和反应要放热热量,属于常见的放热反应;⑤生石灰与水作用制熟石灰,是化合反应,放出热量,属于常见的放热反应;⑥食物因氧化而腐败要放热热量,属于放热反应;属于放热反应的是②③④⑤⑥ ;属于吸热反应的是①;(2)用铜、银与硝酸银设计一个原电池,根据金属的活泼性判断,铜作负极,铜失去电子变成离子进入溶液,发生氧化反应,Cu-2 e - =Cu2+ ;银作正极,银离子得电子生成银单质,发生还原反应,2Ag + +2 e - =2Ag;两个电极反应式相加即得总反应方程式,Cu+2Ag + =2Ag+Cu 2+ .故负极的电极反应式是 Cu-2 e - =Cu2+ ;(3)用锌片、铜片连接后浸入稀硫酸溶液中,构成了原电池,锌为负极,电极反应为:Zn-2e-=Zn2+,铜为正极,电极反应为2H++2e-=H2↑,锌片的质量减少了3.25克,则物质的量为3.25g/65g·mol-1=0.05mol,转移的电子的物质的量为n(e-)=2n(Zn)=2n(H2)=2×0.05mol=0.1mol,则:V(H2)=0.05mol×22.4L·mol-1=1.12L;(4)①由乙烯制1,2-二氯乙烷,为加成反应;②乙烷与氯气光照生成氯乙烷等卤代烃,为取代反应;③乙烯使溴的四氯化碳溶液褪色,发生加成反应;④乙烯通入酸性高锰酸钾溶液,发生氧化还原反应;⑤由苯制取溴苯,发生取代反应;⑥乙烷在空气中燃烧生成水和二氧化碳,为氧化还原反应;⑦由苯制取硝基苯,为取代反应;⑧由苯制取环己烷,为加成反应,故取代反应②⑤⑦;加成反应①③⑧;(5)①公式M = ρ·Vm,其中Vm = 22.4L·mol-1,由已知可以确定出该烃的摩尔质量 M = 3.215 * 22.4 = 72 g·mol-1;(2)∵水的物质的量n(H2O) = 5.4/18 = 0.3 mol,CO2的物质的量n(CO2) = 11/44 = 0.25 mol,烃的物质的量n(烃) = 3.6/72 = 0.05 mol,∴氢原子的物质的量 n(H) = 2·n(H2O) = 2 * 0.3 = 0.6 mol,碳原子的物质的量 n(C) = n(CO2) = 0.25 mol,∴氢原子数N(H) = 0.6/0.05 = 12,碳原子数N(C) = 0.25/0.05 = 5,∴该烃的分子式为C5H12;③若该烃的一氯代物只有一种,则该烃的结构简式为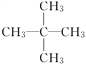 。
。


科目:高中化学 来源: 题型:
【题目】表各组变化中,后者一定包括前者的是( )
A | 化学变化 | 物理变化 |
B | 氧化还原反应 | 分解反应 |
C | 氧化还原反应 | 化合反应 |
D | 中和反应 | 复分解反应 |
A.A
B.B
C.C
D.D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】四种短周期元素在周期表中的相对位置如下表所示,其中Z元素原子核外电子总数是其最外层电子数的3倍。下列说法正确的是( )
X | Y | |
Z | W |
A.元素W位于第三周期第ⅤA族
B.元素Y的氢化物水溶液呈酸性
C.元素X、Z的各种氯化物分子中,各原子均满足8电子稳定结构
D.元素X与氢元素形成的原子个数比为1∶1的化合物有多种
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(I).常温下0.01mol/L HCl溶液由水电离产生的c(H+)与PH=11的CH3COONa溶液中由水电离产生的c(OH-)之比为________。
(II).实验室中配制AgNO3溶液时通常需要向其中加入硝酸目的是______;AgCl在水中存在沉淀溶解平衡:AgCl(s)![]() Ag+(aq)+Cl-(aq)。25℃时,现将足量AgCl分别放入:①100mL蒸馏水;②100mL 0.2molL-1AgNO3溶液;③100mL 0.1molL-1氯化镁溶液;④100mL 0.1molL-1氯化钠溶液.充分搅拌后,相同温度下Ag+浓度由大到小的顺序是______ (填写序号)。
Ag+(aq)+Cl-(aq)。25℃时,现将足量AgCl分别放入:①100mL蒸馏水;②100mL 0.2molL-1AgNO3溶液;③100mL 0.1molL-1氯化镁溶液;④100mL 0.1molL-1氯化钠溶液.充分搅拌后,相同温度下Ag+浓度由大到小的顺序是______ (填写序号)。
(III).己知醋酸和盐酸是日常生活中极为常见的酸,在一定条件下,CH3COOH溶液中存在电离平衡:CH3COOH![]() CH3COO-+H+ △H>0。
CH3COO-+H+ △H>0。
(1) 25 C时,浓度均为0.lmol/L的盐酸和醋酸溶液,下列说法正确的是__________;
①两溶液的pH相同
②两溶液的导电能力相同
③由水电离出的c(OH-)相同
④中和等物质的量的NaOH溶液,消耗两溶液的体积相同
(2)25℃时,在pH=5的稀醋酸溶液中,c(CH3COO-)=_________(填数字表达式);
(3)25℃时,若向氨水中加入稀盐酸至溶液的pH==7,此时c(NH4 +) =amol/L,则c(Cl-)=__________。
(4)25℃时,向体积为VamL pH=3的醋酸溶液中滴加pH=11的NaOH溶液VbmL至溶液恰好呈中性,则Va与的Vb关系是Va____vb (填“>”、“<”或“=”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一个不导热的恒容密闭容器中通入CO(g)和H2O(g),一定条件下使反应CO(g)+H2O(g) ![]() CO2(g)+H2(g)达到平衡状态,正反应速率随时间变化的示意图如下所示。由图可得出的正确结论是
CO2(g)+H2(g)达到平衡状态,正反应速率随时间变化的示意图如下所示。由图可得出的正确结论是
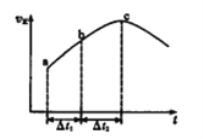
A. 反应物浓度:a点小于c点
B. c点时反应进行的程度最大
C. 该反应的正反应为吸热反应
D. △t1=△t2时,生成H2的物质的量:a~b段小于b~c段
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学中常用图像直观地描述化学反应的进程或结果。下列有些图像描述正确的是

A. 当反应COCl2(g) ![]() CO(g)+Cl2(g);△H>0,达到平衡时①升温②减压③加催化剂都能提高COCl2转化率
CO(g)+Cl2(g);△H>0,达到平衡时①升温②减压③加催化剂都能提高COCl2转化率
B. 图1可能表示压强对可逆反应A(g)+2B(g) ![]() 3C(g)+D(s)的影响,乙的压强大
3C(g)+D(s)的影响,乙的压强大
C. 图2可表示乙酸溶液中通入氨气至过量过程中溶液导电性的变化
D. 据图3,若除去CuSO4溶液中的Fe3+可采用向溶液中加入适量Cu至pH在4左右
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室制备H2和Cl2通常采用下列反应:
Zn+H2SO4===ZnSO4+H2↑
MnO2+4HCl(浓)![]() MnCl2+Cl2↑+2H2O
MnCl2+Cl2↑+2H2O
据此,从下列所给仪器装置中选择制备并收集H2的装置______(填代号)和制备并收集干燥、纯净Cl2的装置______(填代号)。
可选用制备气体的装置:


查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】以下说法正确的是( )
A.物质所含元素化合价升高的反应叫还原反应
B.在氧化还原反应中,失去电子的元素化合价降低
C.物质中某元素失去电子,则此物质是氧化剂
D.还原剂中必定有一种元素被氧化
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将一定量的Cl2通入一定浓度的苛性钾溶液中,两者恰好完全反应(已知反应过程放热),生成物中有三种含氯元素的离子,其中ClO-和ClO![]() 两种离子的物质的量(n)与反应时间(t)的变化示意图如图所示。下列说法正确的是( )
两种离子的物质的量(n)与反应时间(t)的变化示意图如图所示。下列说法正确的是( )
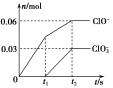
A.苛性钾溶液中KOH的物质的量是0.09 mol
B.ClO![]() 的生成是由于氯气的量的多少引起的
的生成是由于氯气的量的多少引起的
C.在酸性条件下ClO-和ClO![]() 可生成Cl2
可生成Cl2
D.反应中转移电子的物质的量是0.21 mol
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com