
(1)现有如下两个反应:
A.NaOH + HCl =" NaCl" + H2O B.2FeCl3 + Cu = 2FeCl2 + CuCl2
①根据两反应本质判断, 能设计成原电池(填“A”或“B”)。
②如果(A或B)不能,说明其原因
(2)如图所示装置,烧杯中盛有滴有酚酞的NaCl饱和溶液,C(1)、C(2)为多孔石墨电极。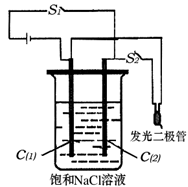
①接通S1后,两极均有气体生成,C(1)附近溶液显 色。装置内发生的总反应化学方程式为 。
②若有11.7g NaCl发生反应,理论上生成Cl2的体积(标准状况)为 。
③反应一段时间后(电极未脱离液面),断开S1,接通S2,观察到二极管发光。此时:C(2)的电极反应式是 。
科目:高中化学 来源:江西省白鹭洲中学2011-2012学年高一下学期期中考试化学试题 题型:022
现有如下两个反应:
A.2NaOH+H2SO4=Na2SO4+2H2O
B.CH4+2O2=CO2+2H2O
(1)根据反应的本质,两个反应都为________反应(放热或吸热),判断两个反应
能否设计为原电池?(填“能或不能”)A________B________
(2)如果能,最好应选择________作电解质溶液(NaOH或H2SO4).则负极电极反
应式:________,正极电极反应式:________.(若均不能则此问不填)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com