
【题目】已知某化学反应A2(g)+2B2(g)===2AB2(g)(AB2的分子结构为B—A—B)的能量变化如图所示,下列有关叙述中正确的是( )
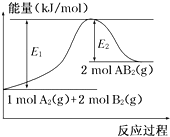
A.该反应的进行一定需要加热
B.该反应的ΔH=-(E1-E2)kJ·mol-1
C.断裂1 molA—A键和2 mol B—B键,放出E1 kJ能量
D.该反应为吸热反应
科目:高中化学 来源: 题型:
【题目】在潮湿的深层土壤中,钢管主要发生厌氧腐蚀,有关厌氧腐蚀的机理有多种,其中一种理论为厌氧细菌可促使SO42-与H2反应生成S2-,加速钢管的腐蚀,其反应原理如图所示。下列说法正确的是( )

A. 正极的电极反应式为:2H2O+O2+4e-=4OH-
B. SO42-与H2的反应可表示为:4H2+SO42--8e S2-+4H2O
S2-+4H2O
C. 钢管腐蚀的直接产物中含有FeS、Fe(OH)2
D. 在钢管表面镀锌或铜可减缓钢管的腐蚀
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在2 L密闭容器内,t℃时发生反应:N2(g)+3H2(g)![]() 2NH3(g),在体系中,n(N2)随时间的变化如下表:
2NH3(g),在体系中,n(N2)随时间的变化如下表:
时间(min) | 0 | 1 | 2 | 3 | 4 | 5 |
N2的物质的量(mol) | 0.20 | 0.10 | 0.08 | 0.06 | 0.06 | 0.06 |
(1)上述反应在第5min时,N2的转化率为_______________________;
(2)用H2表示从0~2 min内该反应的平均速率v(H2)=_____________;
(3)t℃时,在4个均为2L密闭容器中不同投料下进行合成氨反应。根据在相同时间内测定的结果,判断该反应进行快慢的顺序为______________。(用字母填空,下同);
a.v(NH3)=0.05 mol·L-1·min-1 b.v(H2)=0.03 mol·L-1·min-1
c.v(N2)=0.02 mol·L-1·min-1 d.v(H2)=0.00 l mol·L-1·s-1
(4)下列表述能作为反应达到化学平衡状态的标志是_____________。
a.反应速率v(N2):v(H2):v(NH3)=1:3:2
b.各组分的物质的量浓度不再改变
c.混合气体的平均相对分子质量不再改变
d.混合气体的密度不变
e.单位时间内生成n mol N2的同时,生成3n mol H2
f.v(N2)消耗=2v(NH3)消耗
g.单位时间内3mol H—H键断裂的同时2mol N—H键也断裂
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有机化合物M的分子式为C9H12,其中可能含有苯环的结构有![]() 、
、 、
、 等,下列说法错误的是
等,下列说法错误的是
A.有机物M不管是否含有苯环,在一定条件下都能发生氧化反应
B.有机物M的一种结构为![]() 该有机物不能与溴单质发生加成反应
该有机物不能与溴单质发生加成反应
C.除了上述三种物质,M的含苯环的同分异构体还有5种(不考虑立体异构)
D.![]() 与苯互为同系物
与苯互为同系物
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】根据下列实验装置和操作,回答有关问题。

按图中所示装置,用两种不同的操作分别进行实验,观察B容器中的现象。
(1)先夹紧止水夹a,再使A容器中开始反应:①实验中B容器中观察到的现象是_________________;
②B容器中发生反应的离子方程式是____________________________________。
(2)打开止水夹a,使A容器开始反应一段时间后再夹紧止水夹a,①实验中观察到的现象是__________;②B容器中发生反应的离子方程式是________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知2NO2(g) ![]() N2O4(g),在体积相同的A和B两个带活塞的玻璃容器中,如分别注入1/4容积颜色相同的NO2和Br2(气),然后将活塞同时向外拉到1/2处(快速),过一会儿可以看到
N2O4(g),在体积相同的A和B两个带活塞的玻璃容器中,如分别注入1/4容积颜色相同的NO2和Br2(气),然后将活塞同时向外拉到1/2处(快速),过一会儿可以看到
A.A中颜色比B中浅B.A中颜色比B中深
C.A、B中颜色深浅一样D.A、B中颜色都比开始时深
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】肉桂酸是香料、化妆品、医药、塑料和感光树脂等的重要原料。实验室可用苯甲醛和乙酸酐、醋酸钠等原料经下列反应制取肉桂酸,其中苯甲醛为无色油状液体。已知:
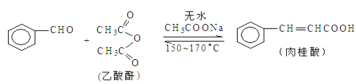 +CH3COOH
+CH3COOH
苯甲醛 | 乙酸酐 | 肉桂酸 | 乙酸 | |
溶解度(25℃,g/100g水) | 0.3 | 遇水易水解成乙酸 | 0.04 | 互溶 |
沸点(℃) | 179.6 | 138.6 | 300 | 118 |
相对分子质量 | 106 | 102 | 148 | 60 |
填空:
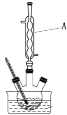
Ⅰ.合成:反应装置如图所示。向三颈烧瓶中先后加入研细的无水醋酸钠、3.6 g苯甲醛和4.2 g乙酸酐,振荡使之混合均匀。在150~170℃加热1小时,保持微沸状态。
(1)仪器A的名称为________,其作用是__________。
(2)该装置加热要控制反应呈微沸状态,如果剧烈沸腾,会导致肉桂酸产率降低,可能的原因是(从平衡移动角度解释)_________。
(3)不能把无水CH3COONa换成CH3COONa·3H2O的原因是_________。
Ⅱ.粗品精制:将上述反应后得到的混合物趁热倒入圆底烧瓶中,进行下列操作:在搅拌下,向反应液中加入20 mL水
A.再慢慢加入碳酸钠溶液
B.然后进行水蒸气蒸馏(已知水蒸气蒸馏是分离提纯有机化合物的重要方法之一,可使待提纯的有机物在低于100℃的情况下随水蒸气一起被蒸馏出来,从而达到分离提纯的目的)
C.待烧瓶内溶液冷却至室温,在搅拌下用加入盐酸酸化,析出大量晶体,过滤,洗涤,干燥。
(4)饱和Na2CO3溶液的作用有_______。水蒸气蒸馏除去的杂质是______。
(5)若得到的肉桂酸晶体产品不纯,应采用____方法可得到纯度更高的产品。
(6)若最后得到纯净的肉桂酸4.3 g,则该反应中的产率是____(保留小数点后一位)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某研究性学习小组设计了一组实验来探究第ⅦA族元素原子的得电子能力强弱规律。下图中A、B、C是三个可供选择制取氯气的装置,装置D的玻璃管中①②③④处依次放置蘸有NaBr溶液、淀粉碘化钾溶液、NaOH浓溶液和品红溶液的棉球。

(1)写出装置B中指定仪器的名称a________,b_________。
(2)实验室制取氯气还可采用如下原理:2KMnO4+16HCl(浓)===2KCl+2MnCl2+5Cl2↑+8H2O。依据该原理需要选择A、B、C装置中的________装置制取氯气。
(3)反应装置的导气管连接装置D的________(填“X”或“Y”)导管,试回答下列问题
①处所发生反应的离子方程式:____________________;
②处的现象:____________________;
③处所发生反应的离子方程式:__________________________。
(4)装置D中④的作用是__________________。
(5)某同学根据①②两处棉球颜色的变化得出结论:Cl、Br、I原子的得电子能力依次减弱。上述实验现象________(填“能”或“不能”)证明该结论、理由是___________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列离子方程式中正确的是
A.用惰性电极电解CuCl2溶液:Cu2++2Cl-+2H2O![]() Cu(OH)2↓+H2↑+Cl2↑
Cu(OH)2↓+H2↑+Cl2↑
B.向FeBr2溶液中通入过量Cl2:2Fe2++4Br﹣+2Cl2=2Fe3++2Br2+4Cl﹣
C.向硫酸氢钾溶液中加入Ba(OH)2溶液至中性:2H++ SO42-+Ba2++2OH﹣=BaSO4↓+2H2O
D.NH4HCO3溶液与过量NaOH溶液反应:NH4+ +OH﹣=NH3↑+H2O
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com