
| A. | 原条件下KCl的溶解度小于ω1g | B. | m1?ω1%-m=m2?ω2% | ||
| C. | ω1一定大于ω2 | D. | m1-m2≤m |
分析 现有某温度下的KCl饱和溶液m1g,溶质的质量分数为ω1%.对其采取某种措施后析出mgKCl晶体,所得母液的质量为m2g,溶质的质量分数为ω2%,晶体KCl析出的条件为降低温度、蒸发水分等.
A.若原溶液为饱和溶液,则溶解度S与质量分数的关系是$\frac{S}{100+S}$×100%=ω1g;
B.m1•ω1%-m=m2•ω2%中满足溶质的质量相等;
C.若原溶液为饱和溶液,条件为降低温度,则冷却将使晶体析出,但温度一定,KCl的溶解度为一定值;
D.若条件只为降低温度使晶体析出,则m 1-m 2=m,若条件只为蒸发水分m(H 2 O) g使晶体析出,则m 1-m 2=m+m(H 2 O),综上所述得m 1-m 2≥m.
解答 解:A.若原溶液为饱和溶液,则溶解度S与质量分数的关系是$\frac{S}{100+S}$×100%=ω1g,得到原条件下KCl的溶解度S大于ω1g,故A错误;
B.依据溶质质量相同列式,原溶液中溶质质量减去析出的氯化钾等于析出晶体后溶液中溶质质量,m1•ω1%-m=m2•ω2%中满足溶质的质量相等,故B正确;
C.若原溶液为饱和溶液,条件为降低温度,则冷却将使晶体析出,但温度一定,KCl的溶解度为一定值,若恢复原温度,ω1一定等于ω2,若降低温度下ω1一定大于ω2,故C错误;
D.若条件只为降低温度使晶体析出,则m 1-m 2=m,若条件只为蒸发水分m(H 2 O) g使晶体析出,则m 1-m 2=m+m(H 2 O),综上所述得m 1-m 2≥m,故D错误;
故选B.
点评 本题考查学生对溶解度等概念的理解能力,溶解度在一定温度下不变,饱和溶液中析出晶体后的溶液在该温度下仍是饱和溶液,掌握概念实质是解题关键,题目难度中等.


科目:高中化学 来源: 题型:选择题
| A. | X、Y同主族 | B. | X原子的半径大于Y原子的半径 | ||
| C. | X的非金属性强于Y的非金属性 | D. | X-的还原性弱于Y-的还原性 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 胶体:豆浆、墨水、血液、生理盐水 | |
| B. | 单质:冰、液氯、臭氧、红磷 | |
| C. | 混合物:矿泉水、84消毒液、铝热剂、四氧化三铁 | |
| D. | 常见的氧化剂:高锰酸钾、氯气、硝酸、氧气 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 在标准状况下,VL水含有的氧原子个数为$\frac{V}{22.4}$NA | |
| B. | CO2通过Na2O2使其增重bg时,反应中转移的电子数为bNA/44个 | |
| C. | 常温下,1L 1 mol•L-1的乙酸溶液中,所含CH3COO-为NA | |
| D. | 常温常压下,0.1 mol氖气含有的电子数为NA |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 (1)电子表所用的某种钮扣电池的电极材料为Zn和Ag2O,电解质溶液为KOH,其电极反应式分别为Zn+2OH--2e-=ZnO+H2O Ag2O+H2O+2e-=2Ag+2OH-
(1)电子表所用的某种钮扣电池的电极材料为Zn和Ag2O,电解质溶液为KOH,其电极反应式分别为Zn+2OH--2e-=ZnO+H2O Ag2O+H2O+2e-=2Ag+2OH-查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①③ | B. | ② | C. | ③④ | D. | ①④ |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
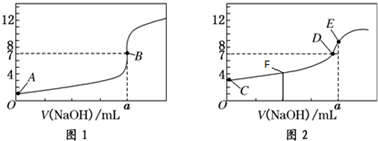
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 在含有等物质的量的H+、Al3+的溶液中,逐滴加入NaOH 溶液:H+、A13+、Al(OH)3 | |
| B. | 在含有等物质的量的FeBr2、FeI2的溶液中,缓慢通入氯气:I-、Br-、Fe2+ | |
| C. | 在含有等物质的量的MgCl2、NH4Cl的溶液中加入NaOH溶液:NH4Cl、MgCl2 | |
| D. | 在含有等物质的量的Fe3+、Cu2+的溶液中加入铁粉:Cu2+、Fe3+ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com