
已知元素X、Y的核电荷数分别是a和b,它们的离子Xm + 和Yn - 的核外电
子排布相同,则下列关系式正确的是( )
A.a = b+m+n B.a = b-m+n C.a = b+m-n D.a=b-m-n
科目:高中化学 来源:2016届辽宁省鞍山市高一下学期期末考试化学(A卷)试卷(解析版) 题型:选择题
丙烯醇(CH2=CH-CH2OH)可发生的化学反应有
①加成 ②氧化 ③酯化 ④加聚 ⑤取代
A.只有①②③B.只有①③④C.只有①②③④D.①②③④⑤
查看答案和解析>>
科目:高中化学 来源:2016届辽宁省抚顺市六校联合体高一下学期期末考试化学试卷(解析版) 题型:选择题
已知X、Y、Z、W四种短周期主族元素在周期表中的相对位置如图所示,下列说法正确的是
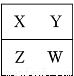
A.W的原子序数可能是Y的原子序数的2倍
B. X可能为氢元素
C.W的气态氢化物的稳定性一定比Y的强
D.X、Y、Z、W四种元素的最外层电子数之和可能为25
查看答案和解析>>
科目:高中化学 来源:2016届福建省福州八市高一下学期期中考试化学试卷(解析版) 题型:选择题
已知下列氧化剂均能氧化+4价的硫元素,为除去稀硫酸中混有的亚硫酸,以得到纯净的稀硫酸,应选用的最合理的氧化剂是( )
A.KMnO4 B.Ca(ClO)2 C.H2O2 D.Cl2
查看答案和解析>>
科目:高中化学 来源:2016届福建省福州八市高一下学期期中考试化学试卷(解析版) 题型:选择题
在硫酸工业生产中,为了有利于SO2的转化,且能充分利用热能,采用了中间有热交换器接触室(见图)。按此密闭体系中气体的流向,则在A处流出的气体为( )
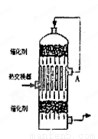
A.SO2 B.SO3、O2 C.SO2、SO3 D.SO2、O2
查看答案和解析>>
科目:高中化学 来源:2016届湖北省孝感市七校联考高一下学期期中考试化学试卷(解析版) 题型:实验题
50 mL 0.50 mol·L-1盐酸与50 mL 0.55 mol·L-1NaOH溶液在如图所示的装置中进行中和反应。通过测定反应过程中所放出的热量可计算中和反应的反应热。
回答下列问题:
(1)从实验装置上看,图中尚缺少的一种玻璃仪器是 。
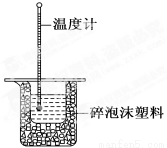
(2)烧杯间填满碎泡沫塑料的作用是 。
(3)大烧杯上如不盖硬纸板,求得的中和反应的反应热的数值 (填“偏大” “偏小”或“无影响”)。
(4)实验中改用55 mL 0.50 mol·L-1盐酸跟50 mL 0.55 mol·L-1NaOH溶液进行反应,与上述实验相比,所放出的热量 (填“相等”或“不相等”)。
(5)用相同浓度和体积的氨水代替NaOH溶液进行上述实验,测得的中和反应的反应热数值会 (填“偏大”“偏小”或“无影响”)
查看答案和解析>>
科目:高中化学 来源:2016届湖北省孝感市七校联考高一下学期期中考试化学试卷(解析版) 题型:选择题
在加入铝粉能放出H 的溶液中,下列各组离子一定不能大量共存的是( )
的溶液中,下列各组离子一定不能大量共存的是( )
A.Na 、Fe
、Fe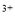 、SO
、SO 、Cl
、Cl
B.Ba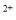 、Mg
、Mg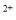 、HCO
、HCO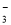 、NO
、NO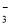
C.Na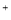 、K
、K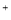 、NO
、NO 、CO
、CO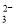
D.K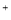 、NO
、NO 、AlO
、AlO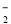 、OH
、OH
查看答案和解析>>
科目:高中化学 来源:2016届海南省第二学期高一期末考试化学试卷(解析版) 题型:填空题
(12分)氮化钠(Na3N)是科学家制备的一种重要化合物,它与水作用可产生NH3 ,请回答:
(1)Na3N的电子式__________________,该化合物是由______________键形成。
(2)Na3N与水反应方程式为____________________________________________。
(3)Na3N放入足量盐酸中生成_______种盐,其化学式为__________________。
(4)比较Na3N中两种粒子的半径:r(Na+)___r(N3-)(填“>”“=”或“<” )
查看答案和解析>>
科目:高中化学 来源:2016届浙江省杭州地区六校高一下学期期中联考化学试卷(解析版) 题型:填空题
在化学反应中,反应物转化成生成物,必然发生能量的变化。
(1)下列说法正确的是 。
A.化学变化中的能量变化主要由化学键变化引起的
B.放热反应发生时不一定要加热,但吸热反应必须要加热才能发生
C.钢铁的吸氧腐蚀和析氢腐蚀的负极反应都为Fe—2e一= Fe2+
D.CaCO3(s) = CaO(s) + CO2(g) ΔH= + 178.5 KJ·mol-1 的意义是表示1mol CaCO3完全分解生成1mol CaO和1mol CO2气体要放出178.5 KJ的热量
(2)101 kPa条件下,氮气和氢气反应生成氨气的能量变化示意图如下:
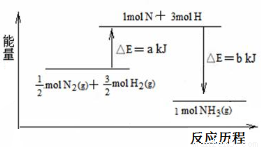
已知:①a=1127;②b=1219
则:1molN2和3molH2参与反应生成2molNH3 (填“吸收”或“放出”)热量 KJ。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com