(2007?淄博三模)A、B、C、D、E五种短周期元素,原子序数依次增大,A、E同主族,A元素的原子半径最小,B元素原子的最外层电子数是内层电子数的2倍,C元素的最高价氧化物的水化物X与其氢化物反应生成一种盐Y,A、B、C、E四种元素都能与D元素形成原子个数比不相同的常见化合物.回答下列问题:
(1)常温下,X、Y的水溶液的pH均为5.则两种水溶液中由水电离出的H
+浓度之比是
10-4:1
10-4:1
.
(2)A、B、D、E四种元素组成的某无机化合物,受热易分解.写出少量该化合物溶液与足量的Ba(OH)
2溶液反应的离子方程式
Ba2++HCO3-+OH-═BaCO3↓+H2O
Ba2++HCO3-+OH-═BaCO3↓+H2O
.
(3)将铝片和镁片用导线相连,插入由A、D、E三种元素组成物质的稀溶液中构成原电池,则负极的电极反应式为
Al+4OH-═AlO2-+2H2O+3e-
Al+4OH-═AlO2-+2H2O+3e-
.
(4)化学反应3A
2(g)+C
2(g)?2CA
3(g).当反应达到平衡时不断改变条件(不改变A
2、C
2和CA
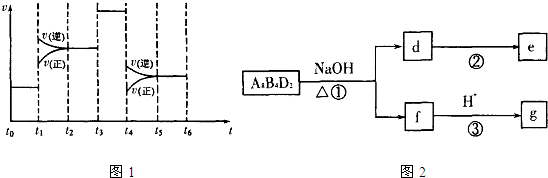
3的量),图1表示反应速率与反应过程的关系,其中表示平衡混合物中CA
3的含量最高的一段时间是
t0~t1
t0~t1
.温度为T℃时,将4a mol A
2和2a mol C
2放入1L密闭容器中,充分反应后测得C
2的转化率为50%,则反应的平衡常数
(5)化合物A
8B
4D
2有如图2转化关系.其中,g是常用调味品的主要成分.写出反应①的化学方程式
CH
3COOC
2H
5+NaOH
CH
3COONa+CH
3CH
2OH
CH
3COOC
2H
5+NaOH
CH
3COONa+CH
3CH
2OH
设计实验方案完成d→e的转化
取一根光洁铜丝绕成螺旋状,放在酒精灯外焰加热,然后伸入d中,反复几次,观察到铜丝由红→黑→红,并闻到液体有刺激性气味
取一根光洁铜丝绕成螺旋状,放在酒精灯外焰加热,然后伸入d中,反复几次,观察到铜丝由红→黑→红,并闻到液体有刺激性气味




 第1卷单元月考期中期末系列答案
第1卷单元月考期中期末系列答案