
高氯酸、硫酸、硝酸和盐酸都是强酸,其酸性在水溶液中差别不大。以下是某温度下这四种酸在冰醋酸中的电离常数
酸 | HClO4 | H2SO4 | HCl | HNO3 |
Ka | 1.6×10-5 | 6.3×10-9 | 1.6×10-9 | 4.2×10-10 |
从以上表格中判断以下说法中不正确的是
A.在冰醋酸中硫酸的电离方程式为H2SO4=2H++SO42-
B.在冰醋酸中高氯酸是这四种酸中最强的酸
C.在冰醋酸中这四种酸都没有完全电离
D.水对于这四种酸的强弱没有区分能力,但醋酸可以区别这四种酸的强弱
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源:2016届黑龙江省高三上12月月考化学试卷(解析版) 题型:选择题
在一个1L的密闭容器中,加入2molA和1molB,发生下述反应: 2A(g) + B(g) 3C(g) + D(s),达到平衡时,C的浓度为1.2mol/L,维持容器的体积和温度不变,按下列配比作为起始物质,达到平衡后,C的浓度还是1.2mol/L的是
3C(g) + D(s),达到平衡时,C的浓度为1.2mol/L,维持容器的体积和温度不变,按下列配比作为起始物质,达到平衡后,C的浓度还是1.2mol/L的是
A.1mol A+0.5mol B+1.5mol C+0.1mol D
B.3mol C+ 0.5mol D
C.2mol A+1mol B+1mol D
D.0.5mol A+0.25mol B+2.25mol C
查看答案和解析>>
科目:高中化学 来源:2016届江西师大附中、临川一中高三上第一次联考化学试卷(解析版) 题型:选择题
在中学化学实验中,对某些化学试剂进行循环使用,可以节省资源、减少污染、降低成本。下列做法不合理的是
选项 | 实验名称 | 回收试剂 | 回收方法 | 回收后用途 |
A | 加热KClO3与MnO2 制氧气 | 二氧化锰 | 溶解、过滤、洗涤、干燥 | 重复使用 |
B | 过氧化钠与水反应 | 氯化钠 | 加入过量盐酸、蒸发、结晶 | 制取实验备用 |
C | 用CCl4萃取溴水中的溴 | 四氯化碳 | 碱液洗涤、分液 | 重复使用 |
D | 浓硫酸的稀释 | 稀硫酸 | 直接密封保存 | 制氢气、硫酸盐等 |
查看答案和解析>>
科目:高中化学 来源:2015-2016学年河北省高一上学期12月月考化学试卷(解析版) 题型:推断题
A、B、C、D、E五种物质的焰色都呈黄色,A、B与水反应都有气体放出,A与水反应放出的气体具有还原性,B与水反应放出的气体具有氧化性,同时都生成溶液C,C与适量的CO2反应生成D,D溶液与过量的CO2反应生成E,E加热能生成D。
(1)写出下列物质的化学式: B ,E 。
(2)写出A→C的化学方程式,并标出电子转移的方向和数目: 。
(3)写出C→D的离子方程式: 。
(4)写出化学方程式:H2O+B→: 。
查看答案和解析>>
科目:高中化学 来源:2015-2016学年江西省高二上学期期中考试化学试卷(解析版) 题型:填空题
研究氨氧化物与悬浮在大气中海盐粒子的相互作用时,涉及如下反应:
2NO2(g)+NaCl(s) NaNO3(s)+ClNO(g) K1 ΔH1<0(Ⅰ)
NaNO3(s)+ClNO(g) K1 ΔH1<0(Ⅰ)
2NO(g)+Cl2(g) 2ClNO(g) K2 ΔH2<0(Ⅱ)
2ClNO(g) K2 ΔH2<0(Ⅱ)
(1)4NO2(g)+2NaCl(s) 2NaNO3(s)+2NO(g)+Cl2(g)的平衡常数K=__________(用K1、K2表示)。
2NaNO3(s)+2NO(g)+Cl2(g)的平衡常数K=__________(用K1、K2表示)。
(2)为研究不同条件对反应(Ⅱ)的影响,在恒温条件下,向2 L恒容密闭容器中加入0.2 mol NO和0.1 mol Cl2,10 min时反应(Ⅱ)达到平衡。测得10 min内v(ClNO)=7.5×10-3 mol·L-1·min-1,则平衡后n(Cl2)=________mol,NO的转化率α1=_______。其他条件保持不变,反应(Ⅱ)在恒压条件下进行,平衡时NO的转化率α2_____α1(填“>”“<”或“=”),平衡常数K2__________(填“增大”“减小”或“不变”)。若要使K2减小,可采取的措施是______________。
(3)实验室可用NaOH溶液吸收NO2,反应为2NO2+2NaOH===NaNO3+NaNO2+H2O。含0.2 mol NaOH的水溶液与0.2 mol NO2恰好完全反应得1 L溶液A,溶液B为0.1 molL的CH3COONa溶液,则两溶液中c(NO3-)、c(NO2-)和c(CH3COO-)由大到小的顺序为_________________。(已知HNO2电离常数Ka=7.1×10-4 mol·L-1,CH3COOH的电离常数Ka=1.7×10-5 mol·L-1)
可使溶液A和溶液B的pH相等的方法是____________。
a.向溶液A中加适量水 b.向溶液A中加适量NaOH
c.向溶液B中加适量水 d.向溶液B中加适量NaOH
查看答案和解析>>
科目:高中化学 来源:2015-2016学年江西省高二上学期12月月考化学试卷(教师版) 题型:选择题
科学家发现用二氧化钛(TiO2)作催化剂可以使水在光照条件下分解制得廉价的氢气,这使氢能源的研究和应用更向前迈 进了一步。下列说法正确的是
进了一步。下列说法正确的是
A、使用二氧化钛作催化剂使水快速分解的同时放出大量热
B、催化剂的作用是降低反应所需要达到的活化能来增大反应的速率
C、该反应的原理是:2H2O 2H2 + O2
2H2 + O2
D、每产生氢气44.8L,转移电子数目为4NA
查看答案和解析>>
科目:高中化学 来源:2014-2015学年江西省高三上学期第六次考试理综化学试卷(解析版) 题型:填空题
近年来,为提高能源利用率,西方提出共生理念——为提高经济效益,人类生产活动尽可能多功能化。共生工程将会大大促进化学工业的发展。
(1)由于共生工程的应用,利用发电厂产生的SO2制成自发电池,其电池反应方程式为:2SO2+O2+2H2O=2H2SO4,该电池电动势为1.06V。实际过程中,将SO2通入电池的 极(填“正”或“负”),负极反应式为 ;用这种方法处理SO2废气的优点是 。
(2)以硫酸工业的SO2尾气、氨水、石灰石、焦炭、碳酸氢铵和氯化钾等为原料,可以合成有重要应用价值的硫化钙、硫酸钾、亚硫酸铵等物质。合成路线如下:
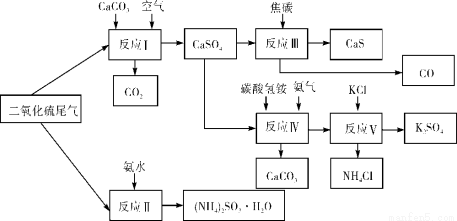
① 生产中,向反应II中的溶液中加入适量还原性很强的对苯二酚等物质,其目的是 。
② 下列有关说法正确的是 (填序号)。
A.反应Ⅰ中需鼓入足量空气,以保证二氧化硫充分氧化生成硫酸钙
B.反应III中发生反应的化学方程式为CaSO4+4C  CaS+4CO↑
CaS+4CO↑
C.反应IV需控制在60~70℃,目的之一是减少碳酸氢铵的分解
D.反应V中的副产物氯化铵可用作氮肥
③ 反应V中选用了40%的乙二醇溶液做溶剂,温度控制在25℃,此时硫酸钾的产率
超过90%,选用40%的乙二醇溶液做溶剂的原因是 。
④(NH4)2SO3可用于电厂等烟道气中脱氮,将氮氧化物转化为氮气,同时生成一种氮肥,形成共生系统。写出二氧化氮与亚硫酸铵反应的化学方程式 。
查看答案和解析>>
科目:高中化学 来源:2016届山东省临沂市高三上学期期中考试化学试卷(解析版) 题型:选择题
下列现象或事实可以用同一原理解释的是
A.浓硫酸和浓盐酸长期露置在空气中浓度均降低
B.氯化铵和碘都可以用加热的方法进行提纯
C.氯水、SO2均能使品红溶液褪色
D.溴蒸汽和NO2气体都能使湿润的淀粉碘化钾试纸变蓝
查看答案和解析>>
科目:高中化学 来源:2015-2016学年四川省高一上期末模拟化学试卷(解析版) 题型:选择题
下列属于电解质的是
A.NaCl溶液 B.蔗糖 C.CuSO4·5H2O D.CO2
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com