
下列有关使用托盘天平的叙述,不正确的是
A.称量前先调节托盘天平的零点;称量时左盘放被称量物,右盘放砝码
B.潮温的或具有腐蚀性的药品,必须放在玻璃器皿里称量,其它固体药品可直接放在天平托盘上称量
C.用托盘天平可以准确称量至0.1g
D.称量完毕后,应把砝码放加砝码盒中
科目:高中化学 来源:2016届江西省高三上学期第一次月考化学试卷(解析版) 题型:实验题
(10分)掌握仪器的名称,组装及使用方法是中学化学实验的基础,如图为两套实验装置。
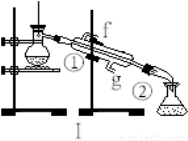
(1)写出下列仪器的名称:
① ② ④ ;
(2)仪器①~④中,使用时必须检查是否漏水的是:(填序号) 。
(3)若利用装置I分离四氯化碳和酒精的混合物,还缺少的仪器有 ,将仪器补充完整后进行的实验操作的名称为 ;该实验操作过程中需要通入冷却水,通入的方向是 (g或f)口进水, (g或f)口出水。
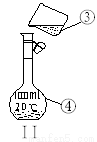
(4)现需配制250 ml 0.2 mol/L NaCl溶液,装置II是某同学转移溶液的示意图,图中的错误是 。
查看答案和解析>>
科目:高中化学 来源:2016届辽宁省大连市高三期初考试化学试卷(解析版) 题型:选择题
仔细分析下列表格中烃的排列规律,判断排列在第15位烃的分子式是
1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9 | …… |
C2H2 | C2H4 | C2H6 | C3H4 | C3H6 | C3H8 | C4H6 | C4H8 | C4H10 | …… |
A.C6H12 B.C6H14 C.C7H12 D.C7H14
查看答案和解析>>
科目:高中化学 来源:2016届江苏省高三上学期开学考试化学试卷(解析版) 题型:选择题
设NA为阿伏加德罗常数的值,下列说法中正确的是
A.标准状况下,22.4L三氯甲烷中共价键数目为4NA
B.1mol碳烯(:CH2)所含电子总数为8NA
C.6.4gCaC2晶体中含有阴阳离子总数为0.2NA
D.1 mol CO2与含2 mol NaOH的溶液反应后,溶液中CO32-数为NA
查看答案和解析>>
科目:高中化学 来源:2016届甘肃省平凉市高三上学期第一次模拟考试化学试卷(解析版) 题型:填空题
(10分)实验需要0.1mol/L NaOH溶液450mL,根据溶液配制中的情况回答下列问题:实验操作如下:
(1)请在下列操作步骤中填写有关的空格:
①用托盘天平称取______g氢氧化钠固体;
②加水溶解,冷却后将溶液沿玻璃棒注入______;
③用少量蒸馏水洗涤烧杯2-3次,并将洗涤液也全部转移到容量瓶中;
④继续向容量瓶中加蒸馏水,直到液面接近刻度线______cm处;
⑤改用______ 逐滴加蒸馏水,使溶液凹面恰好与刻度相切;
⑥盖好容量瓶塞,反复颠倒,摇匀;
⑦将配好的溶液倒入试剂瓶中,贴好标签.
(2)配制过程中,下列情况会使配制结果偏高的是______(填序号)
①定容时俯视刻度线观察液面;
②容量瓶使用时未干燥;
③定容后经振荡、摇匀、静置,发现液面低于刻度线,再加蒸馏水补至刻度线;
④移液后未洗涤烧杯和玻璃棒.
查看答案和解析>>
科目:高中化学 来源:2016届甘肃省平凉市高三上学期第一次模拟考试化学试卷(解析版) 题型:选择题
下列实验中,所采取的分离方法与对应原理都正确的是
选项 | 目的 | 分离方法 | 原理 |
A. | 分离氢氧化铁胶体和氯离子 | 盐析 | 胶体不能透过半透膜,离子能 |
B. | 分离植物油和水的混合物 | 分液 | 二者互不相溶且沸点不同 |
C. | 除去苏打中少量小苏打 | 加热 | 二者的溶解度不同 |
D. | 除去乙醇中的乙酸 | 蒸馏 | 乙醇与乙酸沸点相差较大 |
查看答案和解析>>
科目:高中化学 来源:2016届安徽省高三摸底联考化学试卷(解析版) 题型:选择题
下列装置能达到实验目的的是

A.图1证明酸性:CH3COOH>H2CO3>苯酚 B.图2用排水法收集NO
C.图3萃取碘水中I2,分出水层后的操作 D.图4验证乙烯的生成
查看答案和解析>>
科目:高中化学 来源:2016届山东省枣庄市高三9月阶段性学情检测化学试卷(解析版) 题型:选择题
下列说法可以实现的是
①酸性氧化物在一定条件下均能与碱发生反应
②弱酸与盐溶液反应可以生成强酸
③发生复分解反应,但产物既没有水生成,也没有沉淀和气体生成
④两种酸溶液充分反应后,所得溶液呈中性
⑤有单质参加的反应,但该反应不是氧化还原反应
⑥两种氧化物发生反应有气体生成.
A.①②③④⑤⑥ B.只有①②④⑤ C.只有③④⑤⑥ D.只有②④⑤
查看答案和解析>>
科目:高中化学 来源:2016届江汉油田海南海政学校高三月考化学试卷(解析版) 题型:填空题
(两个选项符合题意,6分)双羟基铝碳酸钠是医疗上常用的一种抑酸剂,其化学式是NaAl(OH)2CO3。关于该物质的说法正确的是( )
A.该物质属于两性氢氧化物
B.该物质是Al(OH)3和Na2CO3的混合物
C.1 mol NaAl(OH)2CO3最多可消耗4 mol H+
D.该药剂不适合于胃溃疡患者服用
18-II(14分)铝是现今人类生产生活中使用广泛性仅次于铁的重要金属。工业上常以“钒土矿”为原料来冶炼金属铝。已知:钒土的主要成分是Al2O3(其中含有Fe2O3、SiO2等杂质)。为了检测某“钒土矿”样中Al2O3的含量,进行了如下实验过程:
①取矿样10.0 g加入过量稀盐酸溶解(假定其他未知成分的杂质都不溶于盐酸,也不和盐酸反应),过滤弃去不溶残渣。
②将滤液稀释并在250 mL容量瓶中定容后,取25.0 mL逐滴滴加2.5 mol·L-1的NaOH溶液,得到如图所示的变化关系。请根据有关数据回答下列问题:
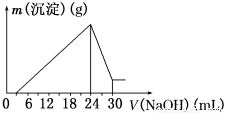
(1)写出滴加NaOH溶液0~3 mL时发生反应的离子方程式:________________。
(2)最后所得不溶于NaOH溶液的沉淀的化学式为______,其物质的量为____________。
(3)该钒土矿样中Al2O3的质量分数为________。
(4)用10.0 t“钒土矿”样提纯所得的Al2O3(提纯过程的损耗忽略不计)进行电解,理论上在 极(填“阴”,“阳”)最多可制得金属铝________t。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com