
A、H2+CuO
| ||||
| B、2Na2O2+2H2O═4NaOH+O2↑ | ||||
C、2KClO3
| ||||
| D、2NaOH+Cl2═NaCl+NaClO+H2O |


科目:高中化学 来源: 题型:
| A、硫离子的核外电子排布式:1s22s22p63s23p6 |
| B、N2的结构式::N≡N: |
C、NaCl的电子式: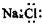 |
D、CO2的分子模型示意图: |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、乙酸乙酯与氢氧化钠溶液反应:CH3COOCH2CH3+2OH-→CH3COO-+CH3CH2O-+H2O | ||
| B、醋酸溶液与新制氢氧化铜反应:2H++Cu(OH)2→Cu2++2H2O | ||
C、苯酚钠溶液中通入少量二氧化碳:2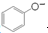 +CO2+H2O +CO2+H2O
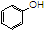 +CO32- +CO32- | ||
D、乙醛溶液与足量的银氨溶液共热:CH3CHO+2[Ag(NH3)2]++2OH-
|
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、CO |
| B、NO |
| C、N2O5 |
| D、Na2O |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、①②③ | B、①③④ |
| C、②④⑤ | D、①④⑥ |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、Ca2+的核外电子排布式为1s22s22p63s23p64s2 |
B、铁原子的价电子轨道排布图: |
| C、某原子的核外电子排布式为1s22s22p63s23p63d54s1,则其成单电子数为2 |
| D、各能级的原子轨道数按s,p,d,f的顺序依次为1、3、5、7 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、燃烧后能生成CO2和H2O的有机物,一定含有碳、氢、氧三种元素 |
| B、所有烷烃中均有碳碳单键 |
| C、属于同分异构体的物质,其分子式相同,分子量相同;但分子量相同的不同物质不一定是同分异构体 |
| D、分子组成相差一个或几个CH2原子团的物质是同系物 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com