
【题目】甲图是部分短周期元素的常见化合价与原子序数的关系图:
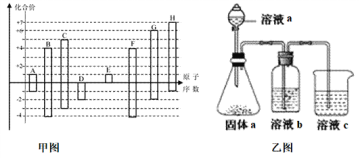
请回答下列问题:
(1)D元素在周期表中的位置为___________,D和G的简单氢化物中沸点高的是___________(写化学式),A和E形成的化合物的电子式为_____________。
(2)D、E、G、H的简单离子半径由大到小的顺序为__________________________。(用化学式表示)
(3)H的最高价氧化物对应的水化物的浓溶液不稳定,受热可分解,产物之一是H的单质,且当有28mol电子转移时,常温共产生9mol气体,写出该反应的化学方程式_________________。
(4)由上述元素中的几种组成a、b、c各物质,某同学设计实验用乙图装置证明元素B、C、F的非金属性强弱(其中溶液b和溶液c均为足量)。
①溶液a和b分别为________,________(填化学式)。
②溶液c中的离子方程式为__________________________________________。
③请从原子结构的角度解释非金属性C>B的原因____________________。
【答案】第二周期第ⅥA族 H2O ![]() S2->Cl->O2->Na+ 4HClO4
S2->Cl->O2->Na+ 4HClO4![]() 2Cl2↑+7O2↑+2H2O HNO3 饱和NaHCO3 SiO32-+CO2+H2O=H2SiO3↓+CO32- 碳和氮两元素位于同一周期,电子层数相同,氮比碳的原子序数大,原子半径小,原子核对最外层电子的吸引能力强,所以氮比碳的非金属性强
2Cl2↑+7O2↑+2H2O HNO3 饱和NaHCO3 SiO32-+CO2+H2O=H2SiO3↓+CO32- 碳和氮两元素位于同一周期,电子层数相同,氮比碳的原子序数大,原子半径小,原子核对最外层电子的吸引能力强,所以氮比碳的非金属性强
【解析】
由图中化合价可知,A有+1、-1价,且原子序数最小,A为H;B的化合价为+4、-4价,B为C元素;C的原子序数小于O,C的化合价有+5、-3价,则C为N;D的化合价只有-2价,没有正化合价,故D为O元素;E的原子序数大于O,且E的化合价为+1价,处于ⅠA族,故E为Na元素;F、B的化合价相同,F与B位于同主族,F的原子序数大,则F为Si;G的最高正价为+6价、最低价为-2,应为S元素;H的最高正价为+7,原子序数最大,则H为Cl。
由上述分析可知:A为H、B为C、C为N、D为O、E为Na、F为Si、G为S、H为Cl,
(1)D元素为O元素,在周期表中的位置为第二周期第ⅥA族,水分子间含氢键,D和G的简单氢化物中沸点高的是H2O,A和E形成的化合物为NaH,为离子化合物,其电子式为![]() 。
。
(2)电子层数越多,离子半价越大,具有相同电子排布的离子中原子序数大的离子半径小,则离子半径为S2->Cl->O2->Na+;
(3)H的最高价氧化物对应的水化物为HClO4,浓溶液不稳定,受热可分解,产物之一是H的单质氯气,且当有28mol电子转移时,常温共产生9mol气体,H为氯气,生成2mol氯气时得到28mol电子,则由电子守恒可知还生成7mol氧气,该反应为4HClO4![]() 2Cl2↑+7O2↑+2H2O;
2Cl2↑+7O2↑+2H2O;
(4)对a、b、c三种物质,某同学设计实验用乙图装置证明元素B、C、F的非金属性强弱由图可知,锥形瓶中发生硝酸与碳酸钙的反应生成二氧化碳,溶液b可除去二氧化碳中挥发的硝酸,试剂为饱和碳酸氢钠,溶液c为硅酸钠,均发生强酸制取弱酸的反应。
①溶液a和b分别为HNO3、饱和NaHCO3。
②碳酸的酸性强于硅酸,溶液c中的离子方程式为SiO32-+CO2+H2O=H2SiO3↓+CO32-。
③从原子结构的角度解释非金属性C>B的原因为:碳和氮两元素位于同一周期,电子层数相同,氮比碳的原子序数大,原子半径小,原子核对最外层电子的吸引能力强,所以氮比碳的非金属性强。


 课堂全解字词句段篇章系列答案
课堂全解字词句段篇章系列答案科目:高中化学 来源: 题型:
【题目】苹果、葡萄、西瓜、山楂是人们普遍喜爱的水果,这些水果富含一种有机物 A,又知A的分子式为C4H6O5。为了弄清该有机物的结构,某兴趣小组的同学做了以下实验:
①该化合物与氢氧化钠溶液反应会生成正盐和酸式盐两种产物;
②该化合物既能与羧酸反应产生有香味的物质,又能与醇反应产生有香味的物质;
③1mol该有机物与足量金属钠反应产生1.5 mol H2;
④利用仪器测知A分子中不含有甲基(—CH3)。请回答下列问题:
(1)根据以上实验结果,对A的结构可作出的判断是________。
A.肯定有碳碳双键 B.有两个羧基
C.肯定有羟基 D.有两个“CH2”基团
(2)有机物A的结构简式为__________________________。
(3)写出A与足量氢氧化钠溶液反应的化学方程式:________________________________。
(4)写出A与金属钠反应的化学方程式:____________________________________。
(5) 写出A与乙酸发生酯化反应的化学方程式:__________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】根据下列图示所得出的结论不正确的是

A. 图甲是CO(g)+H2O(g)![]() CO2(g)+H2(g)的平衡常数与反应温度的关系曲线,说明该反应的ΔH<0
CO2(g)+H2(g)的平衡常数与反应温度的关系曲线,说明该反应的ΔH<0
B. 图乙是室温下H2O2催化分解放出氧气的反应中c(H2O2 )随反应时间变化的曲线,说明随着反应的进行H2O2分解速率逐渐减小
C. 图丙是室温下用0.1000 mol·L1NaOH溶液滴定20.00 mL 0.1000 mol·L1某一元酸HX的滴定曲线,说明HX是一元强酸
D. 图丁是室温下用Na2SO4除去溶液中Ba2+达到沉淀溶解平衡时,溶液中c(Ba2+ )与c(SO42)的关系曲线,说明溶液中c(SO42 )越大c(Ba2+ )越小
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】以天然气为原料合成甲醇。有关热化学方程式如下:
①2CH4(g)+O2(g)=2CO(g)+4H2(g) ΔH1=-70.8 kJ·mol-1
②CO(g)+2H2(g)![]() CH3OH(g) ΔH2
CH3OH(g) ΔH2
③2CH4(g)+O2(g)![]() 2CH3OH(g) ΔH3=-251.0 kJ·mol-1
2CH3OH(g) ΔH3=-251.0 kJ·mol-1
(1)ΔH2=____kJ·mol-1。
(2)在恒容密闭容器里,按物质的量比1:1加入一定量的碳和水蒸气反应生成水煤气。一定条件下达到平衡,当改变反应的某一条件时,下列变化能说明平衡一定向正反应方向移动的是_________。(填序号)
A.正反应速率先增大后减少 B.化学平衡常数K减少
C.再加入一定量碳 D.反应物气体体积分数增大
(3)在体积可变的密闭容器中投入1 mol CO和2 mol H2,在不同条件下发生反应:
CO(g)+2H2(g)![]() CH3OH(g)。实验测得CH3OH的物质的量随温度、压强的变化如图所示。
CH3OH(g)。实验测得CH3OH的物质的量随温度、压强的变化如图所示。

①该反应自发进行的条件是_____________(填“低温”、“高温”或“任意温度”)
②506 K时,反应平衡时H2的转化率为___;压强:p1_____(填“>”“<”或“=”) p2。
③反应速率:N点v正(CO)____(填“>”“<”或“=”)M点v逆(CO)。
④若压强为p1、在1 L恒容密闭容器中进行上述反应(起始投料不变),在不同温度下上述反应的平衡常数的对数(lg K)如图所示。则温度为506 K时,平衡常数K=____(保留三位小数),B、C、D、E四点中能正确表示该反应的lg K与T的关系的点为____。

(4)在2 L恒容密闭容器中充入a(a>0) mol H2、2 mol CO和7.4 mol CH3OH(g),在506 K下进行上述反应。为了使该反应逆向进行,a的范围为________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】I.下列各组物质中,属于同位素的是(填序号,下同)________,属于同素异形体的是________ ,互为同系物的是__________ ,属于同分异构体的是____________ ,属于同种物质的是____________ 。
A O2和O3
B ![]()
C CH3CH2CH2CH3和CH3CH(CH3)2
D CH3CH2CH2CH(C2H5)CH3和CH3CH2CH2CH(CH3)CH2CH3
E  和
和
F  和CH2=CH-CH3
和CH2=CH-CH3
G  和
和
II.乙醇分子中化学键如下:

(1)与金属钠反应时,键________断裂。
(2)催化氧化为醛时,键________断裂。
(3)实验室制备乙烯时,键_________断裂。
(4)写出乙醇和金属镁反应的化学方程式______________________________________________。
(5)写出乙醇和乙酸反应的化学方程式_______________________________________
(6)写出乙醇催化氧化的化学方程式____________________________________________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】向Ba(OH)2和NaOH的混合稀溶液中通入足量的CO2气体,生成沉淀的物质的量(n)和通入CO2气体体积(V)的关系如下图所示,试回答:
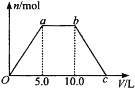
(1)a点之前的反应的离子方程式为________________。
(2)a点到b点之间的反应的离子方程式是________________、________________。
(3)c点二氧化碳体积是________L。
(4)混合稀溶液中Ba(OH)2和NaOH的物质的量之比为____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】反应N2O4(g)2NO2(g)△H=+57kJmol﹣1,在温度为T1、T2时,平衡体系中NO2的体积分数随压强变化的曲线如图所示.下列说法正确的是

A. A、C两点的反应速率:A>C
B. A、C两点气体的颜色:A深,C浅
C. A、B两点气体的平均相对分子质量:A>B
D. B、C两点化学平衡常数:B<C
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室常用下图所示装置制取少量溴苯,并验证其中的一种产物。

请完成下列问题:
(1)在烧瓶a中装的试剂是________、________、________。
(2)导管c的下口能否浸没于液面下____________,理由是____________。
(3)反应过程中在导管c的下口附近可以观察到的现象是有_______出现,这是由于反应生成的_______遇水蒸气而形成的。
(4)反应完毕后,向锥形瓶d中滴加硝酸银溶液有________生成,反应的离子方程式是________
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com