
在水溶液中,下列离子不能将铁氧化成亚铁离子的是
[ ]
|
A. |
B. |
C. |
D. |
| 设计意图:本题是对学生实验能力的综合考查,重点考查了学生对化学实验的分析、归纳和推理能力,反映了学生思维的灵活性和深刻性.
解析:本题涉及的学科内知识有:H2、CO2、H2S、HCl的实验室制法、MnO2催化H2O2分解制O2等;涉及的学科间的知识有物理中的气压与水压等知识. (1)分析题中的装置图:关闭弹簧夹,试管内液面下降,说明试管内气压增大,使漏斗中液面上升,当试管内的气压增大到一定程度,酸液与锌粒脱离,不再产生氢气,反应停止.若打开弹簧夹,试管内气压与外界大气压相等,漏斗中酸液下降又与锌粒接触,产生氢气.所以,此装置可以使反应随时进行、随时停止. (2)由该实验装置的使用原理可知,该装置若漏气,则试管内外便形不成压力差,因此,只要创造条件使试管内外形成压力差便可检验装置的气密性.根据已有装置,可在塞紧塞子和关闭弹簧夹的前提下,向长颈漏斗中加水,若漏气,则漏斗内外不能形成液面差;若气密性良好,则漏斗中液面应比漏斗外液面高. (3)根据实验装置分析,要使制气随制随停,需使固体与液体能随时接触,又能随时脱离,为满足这个要求,固体应在有孔塑料板之上,即为块状固体.若为粉末状,则会掉到试管底部而不能与液体脱离,也就不能使反应停止.实验室制CO2、H2S气体的原料均为块状固体和液体,且均是在常温下反应,故可用此装置,而用MnO2催化过氧化氢分解制O2时,却不可行,原因是催化剂MnO2为粉末状固体. (4)食盐与浓硫酸反应制HCl气体需加热,且食盐为粉末状固体,故不适宜于该装置. 易错点:不能由题中信息归纳出该装置使用的条件:块状固体与液体反应,且能在常温下进行.以致在后面的解答中出错;对H2S、HCl的实验室制法及MnO2催化H2O2制O2的内容不甚明了,导致回答(3)(4)问时失误;因粗心把(3)问中的气体名称写成了化学式;语言组织能力欠佳,在回答(1)(2)问时,词不达意. 答案:(1)关闭弹簧夹时,反应产生的气体使试管内液面上的压力增加,所以液面下降. (2)塞紧橡皮塞,夹紧弹簧夹后,从漏斗中注入一定量的水,使漏斗内的水面高于试管内的水面,停止加水一段时间后,漏斗中与试管中的液面差保持不变,说明装置气密性良好. (3)①二氧化碳 向上排空气法 通入澄清石灰水中,石灰水变浑浊 ②硫化氢 向上排空气法 有臭鸡蛋气味(其他合理答案亦可) ③氧气 排水集气法 使带余烬木条复燃 (4)因为此反应需要加热,且食盐为粉末状固体.  
练习册系列答案
相关习题
科目:高中化学 来源: 题型: X、Y、Z、W是四种短周期元素,X原子M层上的电子数是原子核外电子层数的2倍;Y原子最外层电子数是次外层电子数的2倍;Z元素的单质为双原子分子,Z的氢化物水溶液呈碱性;W元素最高正价是+7价.回答下列问题: (1)元素X原子结构示意图为 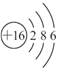  (2)元素Y的一种同位素可测定文物年代,这种同位素的符号是 146C 146C .(3)元素Z能与氢元素形成-1价阴离子,该阴离子的电子总数是 10 10 ,与该离子电子总数相等的Z与氢形成的微粒是NH3、NH4+ NH3、NH4+ .(4)元素W的单质与元素X的低价氧化物在水溶液中反应的离子方程式为 Cl2+SO2+2H2O═4H++2Cl-+SO42- Cl2+SO2+2H2O═4H++2Cl-+SO42- 删除此空 删除此空 .(5)ZW3常温下呈液态,可与水反应生成一种酸和一种碱,反应的化学方程式为 NCl3+4H2O═3HClO+NH3?H2O NCl3+4H2O═3HClO+NH3?H2O .(6)探寻物质的性质差异性是学习的重要方法之一.X、Y、Z、W四种元素的最高价氧化物的水化物中化学性质明显不同于其他三种酸的是 H2CO3 H2CO3 (用酸的分子式表示).查看答案和解析>> 科目:高中化学 来源: 题型: 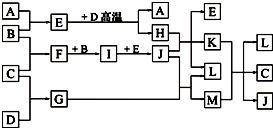 如图,常温下单质A、B为气体,单质C为固体,它们依次分别由短周期元素甲、乙、丙组成,甲元素原子核外电子数等于其电子层数,乙、丙同主族;E常温下为液体,G、H为黑色固体,D是常见金属(反应条件多数略去). 如图,常温下单质A、B为气体,单质C为固体,它们依次分别由短周期元素甲、乙、丙组成,甲元素原子核外电子数等于其电子层数,乙、丙同主族;E常温下为液体,G、H为黑色固体,D是常见金属(反应条件多数略去).回答下列问题: (1)化合物E的沸点高于化合M的沸点,原因是 (2)甲、乙两种元素可以形成两种化合物,其中一种化合物含有4个原子核,该化合物的结构式为 (3)E与D高温反应的化学方程式为 (4)实验室在保存L溶液时,需加入少量D,理由是 (5)已知一定条件下,每1mol F与单质B完全反应生成I放出热量98.0kJ,若2mol F与1mol B在此条件下发生反应,达平衡时,放出热量为176.4kJ,则F的转化率为 ①4mol F、2mol B ②2mol F、2mol B、2mol I ③1mol F、0.5mol B、1mol I ④3mol I、1mol Ne. 查看答案和解析>> 科目:高中化学 来源: 题型: 在水溶液中,下列离子组一定可以大量共存的是( ) A.K+、Na+、Cl-、 C.Al3+、Na+、 查看答案和解析>> 同步练习册答案 湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区 违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com版权声明:本站所有文章,图片来源于网络,著作权及版权归原作者所有,转载无意侵犯版权,如有侵权,请作者速来函告知,我们将尽快处理,联系qq:3310059649。 ICP备案序号: 沪ICP备07509807号-10 鄂公网安备42018502000812号 |