
| A. | 硅是光导纤维的主要成分 | |
| B. | 氢氟酸具有强酸性,可用于蚀刻玻璃 | |
| C. | 碳纤维是一种新型有机高分子材料 | |
| D. | 硅胶可做药品和食品的干燥剂 |
科目:高中化学 来源: 题型:选择题
| A. | KClO3与盐酸 | B. | Cl2与NaOH溶液 | C. | Na2O2和CO2 | D. | Na2S2O3与稀硫酸 |
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
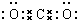 ;元素Z的离子结构示意图为
;元素Z的离子结构示意图为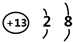 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
 )的缩写代号为PMMA,俗称有机玻璃.下列说法中错误的是( )
)的缩写代号为PMMA,俗称有机玻璃.下列说法中错误的是( )| A. | 聚甲基丙烯酸甲酯属于有机高分子合成材料 | |
| B. | 聚甲基丙烯酸甲酯的分子式可表示为(C5H8O2)n | |
| C. | 合成PMMA的单体是甲基丙烯酸和甲醇 | |
| D. | 甲基丙烯酸甲酯中碳原子可能都处于同一平面 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ③④⑤⑧ | B. | ④⑤⑦⑧ | C. | ④⑤⑧ | D. | ③④⑤⑦⑧ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 体积相等pH=12的氨水和NaOH溶液中和盐酸的能力相同 | |
| B. | 室温下,向NH4HSO4溶液中加入NaOH溶液至中性,则c(SO42-)>c(Na+)>c(NH4+) | |
| C. | 物质的量浓度之比为1:2的CH3COOH和CH3COONa的混合溶液中:2c(CH3COO-)+2c(CH3COOH)=3c(Na+) | |
| D. | 向10ml 0.01mol/L AgNO3溶液中依次滴入2~3滴0.01mol/L NaCl溶液、0.01mol/L NaI溶液,所得沉淀由白色变成黄色,则可推知Kap(AgI)<Kap(AgCl) |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com