
某温度下,将3molA和3molB充入体积为 1L的密闭容器中,发生如下反应:aA(g)+2B(g)?3C(g)+D(g).反应达到平衡后,C的浓度为 3mol/L.压缩容器体积,使容器的体积减小一半,建立新的平衡时,B的浓度为2mol/L.则方程式中a的数值为( )
A.1 B.2 C.3 D.4
科目:高中化学 来源:2015-2016学年山西省高二上12月月考化学试卷(解析版) 题型:实验题
三氯化碘(ICl3,I的化合价为+3价)在药物合成中用途广泛,其熔点:33℃,沸点:73℃,实验室可用如图装置制取ICl3。

(1)制备氯气选用的药品为漂白精固体(主要成分为Ca(ClO)2)和浓盐酸,相关反应的化学方程式为:____________________________;
试剂X为________________、Y为______________;
(2)装置B可用于除杂,也是安全瓶,能监测实验进行时装置C中是否发生堵塞,请写出发生堵塞时B中的现象____________________________;
(3)某同学欲测定ICl3样品中ICl3的纯度,他准确称取ICl3样品10.0g于烧杯中,加入适量水和过量KI晶体,充分反应:ICl3+3KI═2I2+3KCl(样品中杂质不反应).将所得溶液配置成100mL待测液.取25.00mL待测液,用2.0mol/L的Na2S2O3标准液滴定(I2+2S2O32-═2I-+S4O62-),以淀粉溶液作指示剂,达到终点时的现象为____________________________;重复滴定,实验数据记录如下:
滴定次数 | 待测液体积/mL | Na2S2O3标准液体积/mL | |
滴定前读数(mL) | 滴定后读数(mL) | ||
第一次 | 25.00 | 0.50 | 20.40 |
第二次 | 25.00 | 4.00 | 24.10 |
第三次 | 25.00 | 4.20 | 26.70 |
该样品中ICl3的质量分数为_______________(ICl3相对分子质量为233.5)
查看答案和解析>>
科目:高中化学 来源:2016届湖南省高三上学期第五次月考化学试卷(解析版) 题型:选择题
反应3Fe(s)+4H2O(g)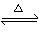 Fe3O4(s)+4H2(g)在一可变容积的密闭容器中进行,下列条件的改变对其反应速率几乎无影响的是
Fe3O4(s)+4H2(g)在一可变容积的密闭容器中进行,下列条件的改变对其反应速率几乎无影响的是
A.把Fe粉变成Fe片
B.将容器的体积缩小一半
C.保持容积不变,充入N2使容器压强增大
D.压强不变,充入N2使容器体积增大
查看答案和解析>>
科目:高中化学 来源:2015-2016学年安徽省高二上期中测试化学试卷(解析版) 题型:选择题
将 4mol A气体和2mol B气体在2L 固定体积的容器中混合并在一定条件下发生如下反应:
2A(g)+B(g) 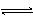 2C(g).若经2s后测得 C 的浓度为 0.6 mol•L-1,现有下列几种说法,其中正确的是( )
2C(g).若经2s后测得 C 的浓度为 0.6 mol•L-1,现有下列几种说法,其中正确的是( )
A. 用物质A表示的反应的平均速率为0.2 mol•L-1•s-1
C. 2s时物质A的转化率为70%
B. 用物质B表示的反应的平均速率为0.1 mol•L-1•s-1
D. 2s时物质B的浓度为0.7 mol•L-1
查看答案和解析>>
科目:高中化学 来源:2015-2016学年安徽省高一上期中测试化学试卷(解析版) 题型:选择题
在一个恒温、恒容密闭容器中,有两个可左右自由滑动的密封隔板(a、b),将容器分成三部分,已知充入的三种气体质量相等,当隔板静止时,容器内气体所占体积如图所示( ),下列说法中错误的是( )

A.若Y是C4H8,则X可能是N2
B.分子数目:X=Z=2Y
C.若X是O2,则Z不可能是CO2
D.气体密度:X=Z=2Y
查看答案和解析>>
科目:高中化学 来源:2015-2016学年广东汕头金山中学高一上12月月考化学卷(解析版) 题型:选择题
将0.4 g NaOH和1.06 g Na2CO3混合并配制成溶液,向溶液中逐滴加入0.1 mol·L-1的盐酸。下列图象能正确表示加入盐酸的体积和生成CO2的物质的量的关系的是
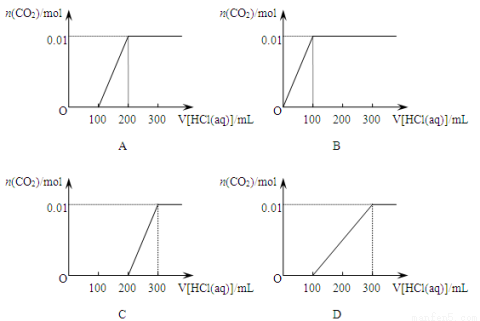
查看答案和解析>>
科目:高中化学 来源:2015-2016学年广东汕头金山中学高二上12月月考化学卷(解析版) 题型:填空题
消除氮氧化物污染有多种方法。
(1)用CH4催化还原氮氧化物可以消除氮氧化物的污染。已知:
①CH4(g)+4NO2(g)=4NO(g)+CO2(g)+2H2O(g)ΔH=-574kJ·mol-1
②CH4(g)+4NO(g)=2N2(g)+CO2(g)+2H2O(g)ΔH=-1160kJ·mol-1
③H2O(g)=H2O(l)ΔH=-44.0kJ·mol-1
写出CH4(g)与NO2(g)反应生成N2(g)、CO2(g)和H2O(l)的热化学方程式__________
(2)用活性炭还原法处理氮氧化物。有关反应为:C(s)+2NO(g) N2(g)+CO2(g)某研究小组向恒容密闭容器加入一定量的活性炭和NO,恒温条件下反应,反应进行到不同时间测得各物质的浓度如下
N2(g)+CO2(g)某研究小组向恒容密闭容器加入一定量的活性炭和NO,恒温条件下反应,反应进行到不同时间测得各物质的浓度如下
浓度/mol·L-1 时间/min | NO | N2 | CO2 |
0 | 0.100 | 0 | 0 |
10 | 0.058 | 0.021 | 0.021 |
20 | 0.040 | 0.030 | 0.030 |
30 | 0.040 | 0.030 | 0.030 |
40 | 0.032 | 0.034 | 0.017 |
50 | 0.032 | 0.034 | 0.017 |
①不能作为判断反应达到化学平衡状态的依据是___ ____
A.容器内CO2的浓度保持不变 B.v正(N2)=2 v正(NO) C.容器内压强保持不变
D.混合气体的密度保持不变 E.混合气体的平均相对分子质量保持不变
②计算该温度下该反应的平衡常数为 (保留两位小数);
③在30 min,改变某一条件,反应重新达到平衡,则改变的条件是____ _ _ ___。
(3) 甲烷燃料电池可以提升能量利用率,下图是利用甲烷燃料电池电解50mL2mol/L的氯化铜溶液的装置示意图:
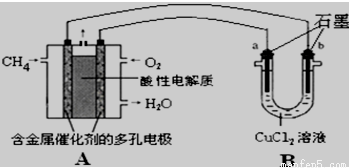
请回答:
①甲烷燃料电池的负极反应式是
②当A中消耗0.15mol氧气时,B中 (用a或b 表示)极增重 g.
查看答案和解析>>
科目:高中化学 来源:2015-2016学年江西省高二上期中(文)化学试卷(解析版) 题型:选择题
用NA表示阿伏加德罗常数,以下各说法中正确的是
A.1mol钠作为还原剂可提供的电子数为NA
B.常温常压下,2.24L四氯化碳中所含氯原子数大于0.4NA
C.0.1mol的铜与足量的浓硫酸反应生成SO2的体积约为2.24L
D.在同温同压下,相同体积的任何气体单质应含有相同的原子数
查看答案和解析>>
科目:高中化学 来源:2016届安徽省高三上学期12月月考化学试卷(解析版) 题型:选择题
一种新药物结构如图所示,下列有关说法正确的是( )
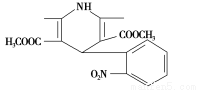
A.该化合物的分子式为C17H17N2O6
B.该化合物的分子中含有三种不同的官能团
C.该化合物的不饱和度为10
D.该化合物能发生水解反应、聚合反应、取代反应、消去反应
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com