
一定温度下,石灰浆中存在下列平衡:Ca(OH)2(s)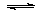 Ca2+(aq)+2OH-(aq),当向一定量的石灰浆中加入少量生石灰后并恢复到原来的温度,下列说法正确的是
Ca2+(aq)+2OH-(aq),当向一定量的石灰浆中加入少量生石灰后并恢复到原来的温度,下列说法正确的是
A.溶液中Ca2+离子数目减少 B.溶液中c(Ca2+)增大
C.溶液的pH增大 D.溶液中溶质的质量分数增大
A
【解析】
试题分析:
石灰浆中存在下列平衡:Ca(OH)2(s)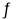 Ca2+(aq)+2OH-(aq),可知石灰浆为Ca(OH)2的饱和溶液,加入少量生石灰(CaO)后,CaO+H2O=Ca(OH)2,消耗水,使石灰浆变为过饱和溶液,有Ca(OH)2的固体析出,所以溶液中Ca2+离子数目减少,剩余石灰浆仍为饱和溶液,即c(Ca2+)、c(OH-)均不变,溶液中溶质的质量分数也不变。
Ca2+(aq)+2OH-(aq),可知石灰浆为Ca(OH)2的饱和溶液,加入少量生石灰(CaO)后,CaO+H2O=Ca(OH)2,消耗水,使石灰浆变为过饱和溶液,有Ca(OH)2的固体析出,所以溶液中Ca2+离子数目减少,剩余石灰浆仍为饱和溶液,即c(Ca2+)、c(OH-)均不变,溶液中溶质的质量分数也不变。
A、因为有Ca(OH)2的固体析出,所以溶液中Ca2+离子数目减少,故A正确;
B、剩余石灰浆仍为饱和溶液,且温度不变,所以c(Ca2+)、c(OH-)均不变,故B不正确;
C、c(OH-)不变,故PH不变,故C不正确;
D、温度不变,剩余石灰浆仍为饱和溶液,溶液中溶质的质量分数也不变,故D不正确。
考点:考查沉淀的溶解平衡
点评;本题考查了沉淀的溶解平衡及其影响因素,难度不大。本题的易错点是忽略了存在沉淀溶解平衡的体系中物质的状态是饱和的。


 尖子生新课堂课时作业系列答案
尖子生新课堂课时作业系列答案科目:高中化学 来源:2014-2015北京市东城区高一上学期期末考试化学试卷(解析版) 题型:选择题
下列反应既属于离子反应,又属于氧化还原反应的是
A.CaO+H2O= B.
B.
C. D.
D.
查看答案和解析>>
科目:高中化学 来源:2014-2015重庆市高一上学期第三次月考化学试卷(解析版) 题型:选择题
氯气与冷的氢氧化钠反应生成NaCl与NaClO,与热的氢氧化钠反应生成NaCl与NaClO3.一定温度下,氯气与氢氧化钠反应生成的NaClO与NaClO3的物质的量之比为2:3,求该反应氧化产物与还原产物的物质的量之比为
A、5/16 B、5/17 C、5/13 D、13/5
查看答案和解析>>
科目:高中化学 来源:2014-2015重庆市高一上学期第三次月考化学试卷(解析版) 题型:选择题
下列物质中,属于纯净物的是
①陶瓷,②水泥,③玻璃,④漂白粉,⑤胆矾,⑥氯水,⑦液氯
A.③⑦ B.③④⑥ C.⑤⑦ D.⑥⑦
查看答案和解析>>
科目:高中化学 来源:2014-2015学年重庆市高二上学期第三次月考化学试卷(解析版) 题型:填空题
(12分)黄铁矿(主要成分为FeS2)是工业制取硫酸的重要原料,其煅烧产物为SO2和Fe3O4。
(1)将0.5molSO2(g)和0.48molO2(g)放入容积为1L的密闭容器中,反应:2SO2(g)+O2(g) 2SO3(g)在一定条件下达到平衡,测得c(SO3)=0.48mol/L。则该条件下SO2的平衡转化率为 。
2SO3(g)在一定条件下达到平衡,测得c(SO3)=0.48mol/L。则该条件下SO2的平衡转化率为 。
(2)若锻烧12gFeS2产生的SO2全部转化为SO3气体时放出19.66kJ热量,产生的SO3与水全部化合生成H2SO4,放出26.06kJ热量,写出SO3气体转化为H2SO4的热化学方程式: 。
(3)将黄铁矿的煅烧产物Fe3O4溶于稀H2SO4后,加入铁粉,可制备FeSO4。酸溶过程中需保持溶液足够酸性,其目的是 。
(4)从吸收塔排出的尾气中SO2先用足量氨水吸收,再用浓硫酸处理,得到较高浓度的SO2和铵盐,写出有关反应的化学方程式: 、 。
SO2既可作为生产硫酸的原料循环再利用,也可用于海水提溴过程中吸收潮湿空气中的Br2,则SO2吸收Br2的离子方程式是 。
查看答案和解析>>
科目:高中化学 来源:2014-2015学年重庆市高二上学期第三次月考化学试卷(解析版) 题型:选择题
25℃和1.01×105 Pa时,反应2N2O5 (g) = 4NO2 (g)+O2 (g) ΔH=+56.76kJ/mol自发进行的原因是
A.是吸热反应 B.是放热反应
C.是熵减少的反应 D.熵增大效应大于能量效应
查看答案和解析>>
科目:高中化学 来源:2014-2015学年重庆市高二上学期第三次月考化学试卷(解析版) 题型:选择题
下列反应能用勒夏特列原理解释的是
A.煅烧粉碎的黄铁矿矿石有利于SO2的生成
B.硫酸生产中用98%的硫酸吸收SO3,而不用H2O或稀硫酸吸收SO3
C.加入催化剂有利于氨的合成
D.工业制取金属钾Na(l)+KCl(l)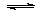 NaCl(l)+K(g)选取适宜的温度,使K变成蒸气从反应混合物中分离出来
NaCl(l)+K(g)选取适宜的温度,使K变成蒸气从反应混合物中分离出来
查看答案和解析>>
科目:高中化学 来源:2014-2015学年北京市丰台区高三第一学期期末练习化学试卷(解析版) 题型:选择题
下列鉴别实验中,所选试剂不合理的是
A.用高锰酸钾酸性溶液鉴别甲苯和己烯
B.用水鉴别苯和四氯化碳
C.用饱和碳酸钠溶液鉴别乙酸和乙酸乙酯
D.用新制的氢氧化铜鉴别乙醛和乙醇
查看答案和解析>>
科目:高中化学 来源:2014-2015山西省忻州市高二上学期期末考试化学试卷(解析版) 题型:选择题
将固体NH4I置于密闭容器中,在一定温度下发生下列反应:
①NH4I(s) NH3(g)+HI(g);②2HI(g)
NH3(g)+HI(g);②2HI(g) H2(g)+I2(g)
H2(g)+I2(g)
达到平衡时,c(H2)=0.25mol/L,c(HI)=5mol/L,
则此温度下反应①的平衡常数(单位:mol2·L-2)为
A.25 B.0.025 C.30.25 D.27.5
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com