
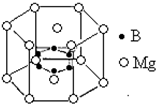
 2001年曾报道,硼镁化合物刷新了金属化合物超导温度的最高记录.该化合晶体结构中的晶胞如图所示.镁原子间形成正六棱柱,六个硼原子位于棱柱内.
2001年曾报道,硼镁化合物刷新了金属化合物超导温度的最高记录.该化合晶体结构中的晶胞如图所示.镁原子间形成正六棱柱,六个硼原子位于棱柱内. .
. 分析 (1)利用均摊法计算晶胞中Mg原子、B原子数目,进而确定化学式,注意顶点原子为6个晶胞共用;
(2)Cu原子核外电子数为29,核外电子排布式为1s22s22p63s23p63d104s1,失去4s能级上的1个电子形成Cu+;
(3)MgF2由镁离子、氟离子构成,应Mg原子、F原子电子式表示其形成过程.
解答 解:(1)镁原子间形成正六棱柱,位于面心与顶点,晶胞中Mg原子数目为2×$\frac{1}{2}$+12×$\frac{1}{6}$=3,六个硼原子位于棱柱内,晶胞中含有6个B原子,故该晶体化学式为MgB2,
故答案为:MgB2;
(2)Cu原子核外电子数为29,核外电子排布式为1s22s22p63s23p63d104s1,失去4s能级上的1个电子形成Cu+,即Cu+的核外电子排布式为1s22s22p63s23p63d10,
故答案为:1s22s22p63s23p63d10;
(3)MgF2由镁离子、氟离子构成,应Mg原子、F原子电子式表示其形成过程为 ,
,
故答案为: .
.
点评 本题是对物质结构的考查,涉及晶胞的计算、核外电子排布、电子式,(1)注意中顶点上的原子被6个晶胞共用而不是8个晶胞,为易错点.


科目:高中化学 来源: 题型:选择题
| A. | 浊液中存在沉淀溶解平衡:AgCl(s)?Ag+(aq)+CI-(aq) | |
| B. | 实验可以证明NH3结合Ag+能力比Cl-强 | |
| C. | 实验表明实验室可用氨水洗涤银镜反应后的试管 | |
| D. | 由资料信息可推知:加浓硝酸后生成的沉淀为AgCl |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 物质W和Z所含的元素可能相同也可能不相同 | |
| B. | 若W是一种气体,它可由氨气的催化氧化直接生成 | |
| C. | 物质W和Z所含有的某种元素,可能是地壳中或空气中含量最高的 | |
| D. | 每转移1mol电子,消耗氧气5.6L |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 铁元素 | B. | 铁单质 | C. | 四氧化三铁 | D. | 三氧化二铁 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com