
(06年北京卷)铝和氢氧化钾都是重要的工业产品。请回答:
(1)工业冶炼铝的化学方程式是__________________________。
(2)铝与氢氧化钾溶液反应的离子方程式是__________________________。
(3)工业品氢氧化钾的溶液中含有某些含氧酸根杂质,可用离子交换膜法电解提纯。电解槽内装有阳离子交换膜(只允许阳离子通过),其工作原理如图所示。

①该电解槽的阳极反应式是__________________________。
②通电开始后,阴极附近溶液pH会增大,请简述原因____________________________
_______________________________________________________________________________________________________________________________________________。
③除去杂质后的氢氧化钾溶液从液化出口_____________(填写“A”或“B”)导出。
答案:(1)2Al2O3![]() 2Al+3O2↑(2)2Al+2OH-+2H2O=2AlO2-+3H2↑(3)①4OH--4e-=2H2O+O2↑ ②H+放电,促进水的电离,OH-浓度增大 ③B
2Al+3O2↑(2)2Al+2OH-+2H2O=2AlO2-+3H2↑(3)①4OH--4e-=2H2O+O2↑ ②H+放电,促进水的电离,OH-浓度增大 ③B
解析:第(1)、(2)小题的化学(或离子)方程式可直接写出。第(3)小题用阳离子交换膜电解法除去工业品氢氧化钾溶液中的杂质(含氧酸根),电解时的电极反应为:
阳极4OH--4e-=2H2O+O2↑
阴极4H++4e-=2H2↑
其中阴极区H+放电,H+浓度减小,使水的电离平衡向右移动促进水的电离,OH-浓度增大。在阴极和阳极之间有阳离子交换膜,只允许阳离子K+和H+通过,这样就在阴极区聚集有大量的K+和OH-,从而纯的氢氧化钾溶液。
高考考点:金属铝的制备与性质;电解。化学工业。
易错点:有的学生审题不清将离子方程式写为化学方程式、将阳极电极反应式误写为阴极电极反应式;语言描述不清。
备考提示:化工生产中涉及的化学知识较多,硫酸的制备、硝酸的制备、合成氨、氯碱工业等,在备考复习时进行系统的总结和归纳。


科目:高中化学 来源: 题型:
(06年北京卷)铝和氢氧化钾都是重要的工业产品。请回答:
(1)工业冶炼铝的化学方程式是__________________________。
(2)铝与氢氧化钾溶液反应的离子方程式是__________________________。
(3)工业品氢氧化钾的溶液中含有某些含氧酸根杂质,可用离子交换膜法电解提纯。电解槽内装有阳离子交换膜(只允许阳离子通过),其工作原理如图所示。
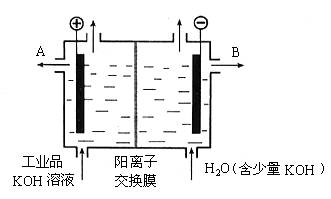
①该电解槽的阳极反应式是__________________________。
②通电开始后,阴极附近溶液pH会增大,请简述原因____________________________
_______________________________________________________________________________________________________________________________________________。
③除去杂质后的氢氧化钾溶液从液化出口_____________(填写“A”或“B”)导出。
查看答案和解析>>
科目:高中化学 来源: 题型:
(06年北京卷)铝和氢氧化钾都是重要的工业产品。请回答:
(1)工业冶炼铝的化学方程式是__________________________。
(2)铝与氢氧化钾溶液反应的离子方程式是__________________________。
(3)工业品氢氧化钾的溶液中含有某些含氧酸根杂质,可用离子交换膜法电解提纯。电解槽内装有阳离子交换膜(只允许阳离子通过),其工作原理如图所示。
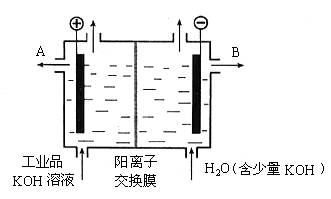
①该电解槽的阳极反应式是__________________________。
②通电开始后,阴极附近溶液pH会增大,请简述原因____________________________
_______________________________________________________________________________________________________________________________________________。
③除去杂质后的氢氧化钾溶液从液化出口_____________(填写“A”或“B”)导出。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com