分析:A、用惰性电极电解饱和食盐水生成氯气、氢气和氢氧化钠;
B、苯酚与碳酸钠溶液反应生成碳酸氢钠;
C、等体积等物质的量浓度的NH4Fe(SO4)2和Ba(OH)2混合时Fe3+和SO42-过量,产物有硫酸钡和Fe(OH)3;
D、碱性条件下反应产物中没有氢离子生成.
解答:解:A、用惰性电极电解饱和食盐水生成氯气、氢气和氢氧化钠,其反应离子方程式为:2Cl
-+2H
2O
Cl
2↑+H
2↑+2OH
-,故A正确
B、苯酚与碳酸钠溶液反应生成碳酸氢钠,其反应离子方程式为:
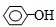
+CO
32-→
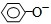
+HCO
3-,故B错误;
C、等体积等物质的量浓度的NH
4Fe(SO
4)
2和Ba(OH)
2混合时Fe
3+和SO
42-过量,产物有硫酸钡和Fe(OH)
3,没有一水合氨生成,所以其反应离子方程式为:2Fe
3++3SO
42-+3Ba
2++6OH
-→3BaSO
4↓+2Fe(OH)
3↓,故C正确;
D、碱性条件下反应产物中没有氢离子生成,所以在强碱性溶液中次氯酸钠与Fe(OH)
3反应生成Na
2FeO
4:4OH
-+3ClO
-+2Fe(OH)
3→2FeO
42-+3Cl
-+5H
2O,故D错误.
故选AC.
点评:本题考查离子反应方程式的正误判断,明确发生的化学反应及离子反应的书写方法即可解答,注意反应物量的关系不同时方程式可能不同,题目难度不大.

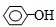 +CO32-→
+CO32-→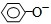 +HCO3-,故B错误;
+HCO3-,故B错误;
