
【题目】用NA表示阿伏加德罗常数的数值,下列说法正确的是( )
A.标准状况下,22.4LCCl4含有NA个分子
B.0.1molAlCl3完全转化为胶体,生成胶体粒子的数目为0.l NA个
C.常温常压下46gNO2和N2O4的混合气体含有3NA个原子
D.0.1molCl2与足量冷的NaOH溶液反应,转移电子数为0.2 NA
 手拉手全优练考卷系列答案
手拉手全优练考卷系列答案科目:高中化学 来源: 题型:
【题目】关于某酸的酸式盐NaHY的水溶液的下列叙述中,正确的是
A. 该酸式盐的水溶液一定显酸性
B. 在该盐溶液中,离子浓度为:c(Na+)>c(Y2-)>c(HY-)>c(OH-)>c(H+)
C. 若HY-能水解,水解方程式为:HY-+H2O![]() Y2-+H3O+
Y2-+H3O+
D. 若HY-能电离,电离方程式为:HY-+H2O![]() Y2-+H3O+
Y2-+H3O+
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各组元素性质和原子结构递变情况不正确的是( )
A. Li、Be、B原子最外层电子数依次增多 B. P、S、Cl元素最高正化合价依次增大
C. N、O、F原子半径依次增大 D. Na、K、Rb的电子层数依次增多
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列离子方程式中,正确的是( )
A.铁与稀硫酸反应 Fe+2H+═Fe3++H2↑
B.氯化铝溶液与氨水反应:Al3++3OH﹣═Al(OH)3↓
C.碳酸钙与稀盐酸反应:CO ![]() +2H+═H2O+CO2↑
+2H+═H2O+CO2↑
D.氢氧化铝与足量盐酸反应 Al(OH)3+3H+═Al3++3H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定条件下,反应N2(g)+3H2(g)2NH3(g)在10L的密闭容器中进行,测得2min内N2的物质的量由20mol减小到8mol,则2min内用NH3表示的反应速率为( )
A.1.2mol/(Lmin)
B.6.0mol/(Lmin)
C.0.6mol/(Lmin)
D.0.4mol/(Lmin)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列装置所示的实验中,能达到实验目的是( )
A.![]() 从Mg(OH)2悬浊液中分离出Mg(OH)2
从Mg(OH)2悬浊液中分离出Mg(OH)2
B.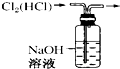 除去Cl2中的HCl
除去Cl2中的HCl
C.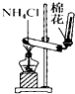 实验室制氨气
实验室制氨气
D. 排水法收集NO
排水法收集NO
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用可溶性钡盐检验SO42-的存在时,先在待测溶液中加入盐酸,其作用是( )
A. 排除SO42-以外的其他弱酸根阴离子及Ag+的干扰
B. 形成的沉淀纯度更高
C. 只是为了排除CO32-的影响
D. 形成较多的白色沉淀
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】反应Fe+H2SO4═FeSO4+H2↑的能量变化趋势,如图所示: 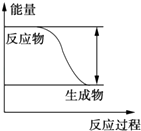
(1)该反应为反应(填“吸热”或“放热”).
(2)若要使该反应的反应速率加快,下列措施可行的是(填字母).
A.改铁片为铁粉
B.改稀硫酸为98%的浓硫酸
C.升高温度
(3)若将上述反应设计成原电池,铜为原电池某一极材料,则铜为极(填“正”或“负”); 铜电极上发生的电极反应为 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】关于乙酸的下列说法不正确的是( )
A.乙酸是一种重要的有机酸,是具有强烈刺激性气味的液体
B.乙酸分子中含有四个氢原子,所以乙酸是四元酸
C.无水乙酸又称冰醋酸,它是纯净物
D.乙酸易溶于水和乙醇
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com