
科目:高中化学 来源: 题型:
| 5 |
| 2 |
| 5 |
| 2 |
查看答案和解析>>
科目:高中化学 来源: 题型:阅读理解
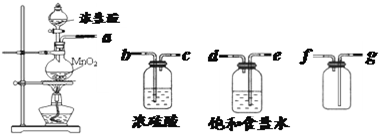
| 实验方法 | 实验现象 | 结论 |
| 在溶液中加 KSCN溶液 |
固体物质中有FeCl3 | |
| 向a溶液中滴加 酸性KMnO4溶液 |
KMnO4溶液色 不褪色 |
固体物质中不含______ |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:
化学反应过程中发生物质变化的同时,常常伴有能量的变化.这种能量的变化常以热能的形式表现出来,叫做反应热.由于反应的情况不同,反应热可以分为许多种,如燃烧热和中和热,等等.
(1)下列ΔH表示物质燃烧热的是________;表示物质中和热的是________.(填ΔH1、ΔH2 和ΔH3等)
A.2H2(g)+O2(g)=2H2O(l) ΔH1;
B.C(s)+1/2O2(g)=CO(g) ΔH2
C.CH4(g)+2O2(g)=CO2(g)+2H2O(g) ΔH3;
D.C(s)+O2(g)=CO2(g) ΔH4;
E.C6H12O6(s)+6O2(g)=6CO2(g)+6H2O(l) ΔH5
F.NaOH(aq)+HCl(aq)=NaCl(aq)+H2O(l) ΔH6
G.2NaOH(aq)+H2SO4(aq)=Na2SO4(aq)+2H2O(l); ΔH7
(2)2.00gC2H2气体完全燃烧生成液态水和CO2,放出99.6 kJ的热量.写出该反应的热化学方程式: 。
(3)充分燃烧一定量的丁烷放出的热量大小为Q,生成的CO2恰好与5 mol/L100mL KOH溶液完全反应.求燃烧1 mol丁烷放出的热量(设其数值为X) 。
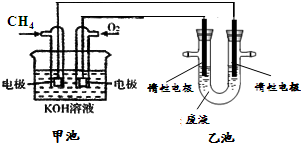
(4)碳和碳的化合物在生产、生活中的应用非常广泛,“低碳生活”已成潮流,清洁能源的开发、煤的综合利用等是实现“低碳生活”的重要途径。甲烷是一种重要的清洁燃料,燃烧放出大量的热,可直接作为能源用于人类的生产和生活。
已知:①2CH4(g)+3O2(g)=2CO(g)+4H2O(l) △H1= —1214 kJ/mol
②2CO(g)+O2(g)=2CO2(g) △H2= —566 kJ/mol
则表示甲烷燃烧热的热化学方程式 ;
请从化学反应的本质解释甲烷燃烧放出热量的原因: 。
查看答案和解析>>
科目:高中化学 来源:2012-2013学年四川省雅安中学高二(上)期中化学试卷(解析版) 题型:填空题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com