
ȼ�ϵ����һ�����͵�����Ⱦ������������Ч�ʵķ����豸����һ�ֺ��з�չDZ��������Դ������Ҫ��ȼ�ϡ����������缫�͵������ɣ�ȼ�ϵ�صĽṹ�ʹ�ͳ���һ�����������缫�������缫������ʷָ������Ի�ԭ����������ȼ�ϣ�Ϊ������Ӧ�����������������е������ȣ�Ϊ�����������ȼ�ϵ���У�������ȼ����ͨ�������¾����ڵ缫�Ͻ��е缫��Ӧ��һ���ö�������������缫���ϣ�������еĵ����Ϊ�л��߷��Ӹ߾�������Խ������ӣ�
��1��ȼ�ϵ�صĵ缫�ڳ��������¾��ܳ��������缫��Ӧ��д������ȼ�ϵ���еĵ缫��Ӧʽ������______________������______________��
��2������ȼ�ϵ�ؿ���Ϊ���˺���������ѡ��أ�һ����Ҫԭ�������ڲ������������Ĺ��������ɵIJ�����ˮ�������ý������Ա����ˮ���⣬����Ա������Щ�ϳ�ˮͨ������ϵͳ�����ڱ�___________���գ�
 �»����ܶ�Ա��ϵ�д�
�»����ܶ�Ա��ϵ�д� ����ͼ����ּ��������ҵ֣�ݴ�ѧ������ϵ�д�
����ͼ����ּ��������ҵ֣�ݴ�ѧ������ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
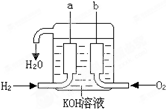
 ��������������ɴ���ʹ�õ�����ȼ�ϵ����һ�����͵Ļ�ѧ��Դ���乹����ͼ��ʾ��a��b�����缫���ɶ��̼�Ƴɣ�ͨ��������ɿ�϶���ݳ������ڵ缫����ŵ磮
��������������ɴ���ʹ�õ�����ȼ�ϵ����һ�����͵Ļ�ѧ��Դ���乹����ͼ��ʾ��a��b�����缫���ɶ��̼�Ƴɣ�ͨ��������ɿ�϶���ݳ������ڵ缫����ŵ磮�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
 �ҹ������ۡ�������ɴ��ɹ����䲢���գ����ҹ�����ʷ�ϵ���̱��� �ɴ���ʹ�õ�����ȼ�ϵ����һ�����͵Ļ�ѧ��Դ�������и��ܡ���㡢����Ⱦ�������ص㣮����ȼ�ϵ�صĹ�������ͼ��ʾ�������缫���ɶ����̼�Ƴɣ�ͨ��������ɿ�϶�ݳ����ڵ缫����ŵ磮
�ҹ������ۡ�������ɴ��ɹ����䲢���գ����ҹ�����ʷ�ϵ���̱��� �ɴ���ʹ�õ�����ȼ�ϵ����һ�����͵Ļ�ѧ��Դ�������и��ܡ���㡢����Ⱦ�������ص㣮����ȼ�ϵ�صĹ�������ͼ��ʾ�������缫���ɶ����̼�Ƴɣ�ͨ��������ɿ�϶�ݳ����ڵ缫����ŵ磮�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
 ��������������ɴ���ʹ�õ�����ȼ�ϵ����һ�����͵Ļ�ѧ��Դ������Ϊ21���͵����ǵ�أ��乹����ͼ��ʾ�������缫���ɶ����̼�Ƴɣ�ͨ��������ɿ�϶���ݳ������ڵ缫����ŵ磮
��������������ɴ���ʹ�õ�����ȼ�ϵ����һ�����͵Ļ�ѧ��Դ������Ϊ21���͵����ǵ�أ��乹����ͼ��ʾ�������缫���ɶ����̼�Ƴɣ�ͨ��������ɿ�϶���ݳ������ڵ缫����ŵ磮�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
 ��������������ɴ���ʹ�õ�����ȼ�ϵ����һ�����͵Ļ�ѧ��أ��乹����ͼ��ʾ�������缫���ɶ����̼�Ƴɣ�ͨ��������ɿ�϶���ݳ������ڵ缫����ŵ磮
��������������ɴ���ʹ�õ�����ȼ�ϵ����һ�����͵Ļ�ѧ��أ��乹����ͼ��ʾ�������缫���ɶ����̼�Ƴɣ�ͨ��������ɿ�϶���ݳ������ڵ缫����ŵ磮�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2012��³�ư���л�ѧѡ��4 1.3��ѧ��ת��Ϊ����-�����ϰ���������棩 ���ͣ������
��������������ɴ���ʹ�õ�����ȼ�ϵ����һ�����͵Ļ�ѧ��أ��乹����ͼ��ʾ�������缫���ɶ����̼�Ƴɣ�ͨ��������ɿ�϶���ݳ������ڵ缫����ŵ硣

��1��a���� ����b���� �����缫
��Ӧʽ�ֱ�Ϊ �� ��
��2���ɴ����Ա��������ˮ��ȼ�ϵ���ṩ����֪���ֵ�ط�1�ȵ�ʱ������350gˮ���Լ�������ת���ʡ�
 [2H2(g)+O2(g)
2H2O(l)+572kJ]
[2H2(g)+O2(g)
2H2O(l)+572kJ]
��3�����ֵ�ص������ѹΪ1.2V��Ҫʹ����1.2V��1.5W��С������������0.5h��Ӧ���ı�״���µ�H2��������
��4��������ȼ�ϵ�����ȼ�ϣ���Ȼʹ�÷��㣬ȴ�ܵ��۸����Դ�����ơ����õ�ȼ�ϣ�������ijЩ̼�⻯�������飨��Ȼ���������͵ȡ���д����ͼ��H2����CH4ʱ�����ɵļ���ȼ�ϵ����a���ĵ缫��Ӧʽ�� ����ʱ������ܵķ�Ӧ����ʽΪ ��
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com