
电石中的碳化钙和水能完全反应:CaC2+2H2O→C2H2↑+Ca(OH)2使反应产生的气体排水,测量排出水的体积,可计算出标准状况乙炔的体积,从而可测定电石中碳化钙的含量.
(1)若用下图仪器和导管组装实验装置:
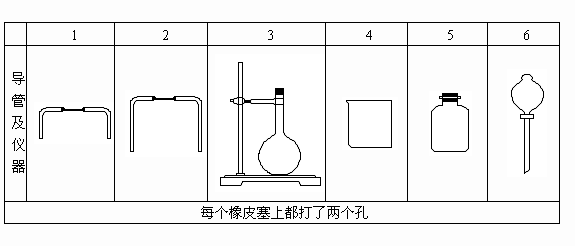
如果所制气体流向从左向右时,上述仪器和导管从左到右直接连接的顺序(填各仪器、导管的序号)是________接________接________接________接________接________.
(2)仪器连接好后,进行实验时,有下列操作(每项操作只进行一次):
①称取一定量电石,置于仪器中,塞紧橡皮塞
②检查装置的气密性
③在仪器6和5中注入适量水
④待仪器3恢复到室温时,量取仪器4中水的体积(导管2中的水忽略不计)
⑤慢慢开启仪器6的活塞,使水逐滴滴下,至不发生气体时,关闭活塞
正确的操作顺序是________(用操作编号填写).
(3)若实验产生的气体有难闻的气味,且测定结果偏大,是因为电石中含有________杂质.
(4)若实验时称取的电石为1.60g,测量排出水的体积后,折算成标准状况乙炔的体积为448ml,此电石中碳化钙的质量分数是________.
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
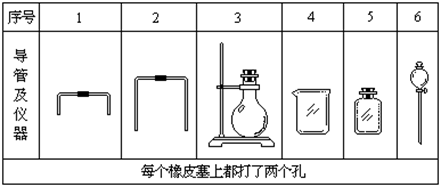
(4分)电石中的碳化钙和水能完全反应,使反应产生的气体排水,测量出水的体积,可计算出标准状况下乙炔的体积,从而测定电石中碳化钙的含量:(1)若用下列仪器和导管组装实验装置:
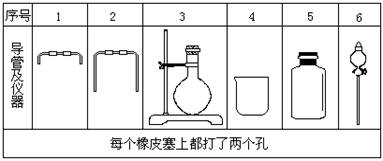
(1)如果所制气体流向从左向右时,上述仪器和导管从从上到下,从左到右直接连接的顺序(填各仪器,导管的序号)是 接 接 接 接 接 。
(2)碳化钙和水反应的化学方程式
查看答案和解析>>
科目:高中化学 来源:2010—2011年云南潞西市芒市中学高二上学期期末考试化学试卷 题型:实验题
(4分)电石中的碳化钙和水能完全反应,使反应产生的气体排水,测量出水的体积,可计算出标准状况下乙炔的体积,从而测定电石中碳化钙的含量:(1)若用下列仪器和导管组装实验装置: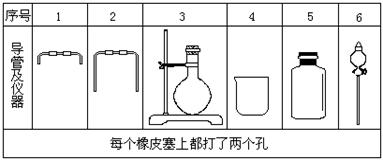
(1)如果所制气体流向从左向右时,上述仪器和导管从从上到下,从左到右直接连接的顺序(填各仪器,导管的序号)是 接 接 接 接 接 。
(2)碳化钙和水反应的化学方程式
查看答案和解析>>
科目:高中化学 来源:2010-2011年云南潞西市高二上学期期末考试化学试卷 题型:实验题
(4分)电石中的碳化钙和水能完全反应,使反应产生的气体排水,测量出水的体积,可计算出标准状况下乙炔的体积,从而测定电石中碳化钙的含量:(1)若用下列仪器和导管组装实验装置:
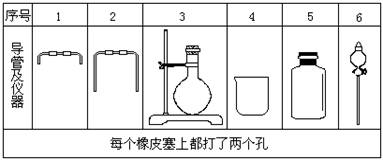
(1)如果所制气体流向从左向右时,上述仪器和导管从从上到下,从左到右直接连接的顺序(填各仪器,导管的序号)是 接 接 接 接 接 。
(2)碳化钙和水反应的化学方程式
查看答案和解析>>
科目:高中化学 来源: 题型:
电石中的碳化钙和水能完全反应:
CaC2+2H2O=C2H2↑+Ca(OH)2
使反应产生的气体排水,测量排出水的体积,可计算出标准状况乙炔的体积,从而可测定电石中碳化钙的含量。
(1)若用下列仪器和导管组装实验装置:
如果所制气体流向从左向右时,上述仪器和导管从左到右直接连接的顺序(填各仪器、导管的序号)是:(6)接(3)接( )接( )接( )接(4)。
(2)仪器连接好后,进行实验时,有下列操作(每项操作只进行一次):
①称取一定量电石,置于仪器3中,塞紧橡皮塞。
②检查装置的气密性。
③在仪器6和5中注入适量水。
④待仪器3恢复到室温时,量取仪器4中水的体积(导管2中的水忽略不计)。
⑤慢慢开启仪器6的活塞,使水逐滴滴下,至不发生气体时,关闭活塞。
正确的操作顺序(用操作编号填写)是 。
(3)CaC2是 (填“离子”或“共价”)化合物,它的电子式为
(4)若实验产生的气体有难闻的气味,且测定结果偏大,这是因为电石中含有 杂质。
(5)若实验时称取电石1.60g,测量排出水的体积后,折算成标准状况乙炔的体积为448mL,此电石中碳化钙的质量分数是 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com