
| A. | 增大N2O4的浓度 | B. | 增大NO2的浓度 | C. | 升高体系的温度 | D. | 减小压强 |
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:选择题
| A. | SO2+Cl2+2H2O=H2SO4+2HCl | B. | 3CO2+4NaOH=2NaHCO3+Na2CO3+H2O | ||
| C. | Ca(ClO)2+CO2+H2O=CaCO3↓+2HClO | D. | 2NO2+2NaOH=NaNO2+NaNO3+H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 75 mL 1.5 mol•L-1的MgCl2溶液 | B. | 75 mL 4 mol•L-1的NH4Cl溶液 | ||
| C. | 150 mL 2 mol•L-1的KCl溶液 | D. | 150 mL 1 mol•L-1的NaCl溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
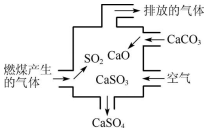
| A. | 使用此装置可以减少导致酸雨的气体的排放 | |
| B. | 该装置内只发生了化合反应 | |
| C. | 总反应可表示为2SO2+2CaCO3+O2?2CaSO4+2CO2 | |
| D. | 若排放的气体能使澄清石灰水变浑浊,说明该气体中含有SO2 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
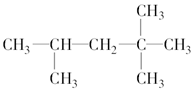 2,2,4-三甲基戊烷
2,2,4-三甲基戊烷 3,4-二甲基己烷
3,4-二甲基己烷查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1:1:1 | B. | 3:4:3 | C. | 1:4:9 | D. | 1:2:3 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 溶液、胶体和悬浊液三种分散系的本质区别是分散质微粒直径的大小 | |
| B. | 甲醇和氧气以及KOH溶液构成的新型燃料电池中,其正极上发生的反应为:CH3OH-6e-+8OH-=CO32-+6H2O | |
| C. | 在铁上镀铜时,金属铜作阴极 | |
| D. | 电解法精炼铜时,电解质溶液中铜离子浓度一定不变 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 氯气是一种重要的化工原料,广泛应用于自来水的消毒和农药的生产等方面 | |
| B. | 钠和钾的合金在常温下是液体,可用于快中子反应堆作热交换剂 | |
| C. | 用二氧化硅制造的光导纤维具有很强的导电能力,可用于制作光缆 | |
| D. | 化肥的生产、金属矿石的处理、金属材料的表面清洗等都可能用到硫酸 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com