
某课外兴趣小组为探究铜跟浓硫酸反应情况,用下图所示装置进行实验。已知:①SO2难溶于饱和亚硫酸氢钠溶液;②SO2能与酸性高锰酸钾溶液发生氧化还原反应使之褪色(化学方程式为5SO2+2KMnO4+2H2O=K2SO4+2MnSO4+2H2SO4)。
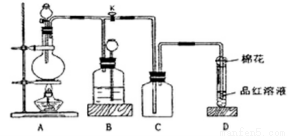
回答下列问题(注:E为止水夹,F为旋塞):
(1)检查A装置的气密性的方法 。
(2)装置A中反应的化学方程式为 。
(3)装置D中试管口放置的棉花应蘸有NaOH溶液,
其作用是 。
(4)装置B具有贮存气体的作用。当D处有明显的现象后,关闭旋塞F并移去酒精灯,由于余热的作用,A处仍有气体产生,此时B中的现象是 ,B中应放置的液体是(填字母) 。
A. 水 B. 饱和NaHSO3溶液 C. 酸性KMnO4溶液 D. NaOH溶液
(5)该小组学生做了如下实验:取一定质量的铜片和一定体积18.4 mol·L-1的浓硫酸放在圆底烧瓶中共热,直到反应完毕,发现烧瓶中没有铜片剩余。往反应后的溶液中加入足量的BaCl2溶液,获得沉淀3.495 g;产生的气体恰好使200ml 0.01mol·L-1的酸性高锰酸钾溶液褪色,则实验中取用的硫酸的物质的量为 。
(1)夹紧水夹E,关闭分液漏斗旋塞,往分液漏斗中加水,打开分液漏斗旋塞,若漏斗中水滴入部分后便停止,证明气密性好。若水一直滴入,则气密性不好。
(2)H2SO4(浓)+Cu CuSO4+SO2↑+2H2O
CuSO4+SO2↑+2H2O
(3)吸收尾气中SO2,防止污染;
(4)瓶中液面下降,漏斗中液面上升; B
(5)0.02mol;
【解析】
试题分析:(1)检查A装置的气密性的方法是夹紧水夹E,关闭分液漏斗旋塞,往分液漏斗中加水,打开分液漏斗旋塞,若漏斗中水滴入部分后便停止,证明气密性好。若水一直滴入,则气密性不好。(2)在装置A浓 与Cu发生反应,化学方程式为H2SO4(浓)+Cu CuSO4+SO2↑+2H2O. (3)SO2是大气污染物,如不处理,容易导致大气污染。所以在装置D中试管口放置的棉花应蘸有NaOH溶液,其作用是吸收尾气中SO2,防止污染;(4)装置B具有贮存气体的作用。当D处有明显的现象后,关闭旋塞F并移去酒精灯,由于余热的作用,A处仍有气体产生,此时B中的现象是瓶中液面下降,漏斗中液面上升至一定的高度。由于SO2难溶于饱和亚硫酸氢钠溶液; SO2能与酸性高锰酸钾溶液发生氧化还原反应使之褪色,而且容易溶解在水中。所以B中应放置的液体是饱和NaHSO3溶液。选项为B。根据S守恒可得n(H2SO4)=n(SO42-)+n(SO2)。n(SO42-)=3.495 g÷233g/mol=0.015mol;根据方程式5SO2+ 2KMnO4+2H2O=K2SO4+2MnSO4+2H2SO4可得n(SO2)= 5/2×n(KMnO4)= 5/2×0.2L×0.01mol/L=0.005mol.所以n(H2SO4)=0.02mol。
CuSO4+SO2↑+2H2O. (3)SO2是大气污染物,如不处理,容易导致大气污染。所以在装置D中试管口放置的棉花应蘸有NaOH溶液,其作用是吸收尾气中SO2,防止污染;(4)装置B具有贮存气体的作用。当D处有明显的现象后,关闭旋塞F并移去酒精灯,由于余热的作用,A处仍有气体产生,此时B中的现象是瓶中液面下降,漏斗中液面上升至一定的高度。由于SO2难溶于饱和亚硫酸氢钠溶液; SO2能与酸性高锰酸钾溶液发生氧化还原反应使之褪色,而且容易溶解在水中。所以B中应放置的液体是饱和NaHSO3溶液。选项为B。根据S守恒可得n(H2SO4)=n(SO42-)+n(SO2)。n(SO42-)=3.495 g÷233g/mol=0.015mol;根据方程式5SO2+ 2KMnO4+2H2O=K2SO4+2MnSO4+2H2SO4可得n(SO2)= 5/2×n(KMnO4)= 5/2×0.2L×0.01mol/L=0.005mol.所以n(H2SO4)=0.02mol。
考点:考查关于浓硫酸与铜反应原理、装置气密性的检查、物质的应用、物质的量的有关计算等知识。


 名师导航单元期末冲刺100分系列答案
名师导航单元期末冲刺100分系列答案 名校名卷单元同步训练测试题系列答案
名校名卷单元同步训练测试题系列答案科目:高中化学 来源:2016届辽宁省高一上学期12月月考化学试卷(解析版) 题型:选择题
下列各项操作中,不发生“先产生沉淀,然后沉淀又溶解”现象的是( )
①向饱和碳酸钠溶液中通入过量的CO2
②向Fe(OH)3胶体中逐滴加入过量的稀盐酸
③向NaAlO2溶液中通入过量的CO2
④向澄清石灰水中通入缓慢过量的CO2
A.①② B.①④ C.①③ D.②③
查看答案和解析>>
科目:高中化学 来源:2016届辽宁省大连市高一上学期期末考试化学试卷(解析版) 题型:选择题
配制一定体积、一定物质的量浓度的溶液时,下列操作会使配得的溶液浓度偏小的是
A.容量瓶中原有少量蒸馏水
B.定容时观察液面仰视
C.转移溶液时,没有等溶液冷却至室温
D.胶头滴管加水定容时,有少量水滴到容量瓶外
查看答案和解析>>
科目:高中化学 来源:2016届贵州省高一上学期期中考试化学试卷(解析版) 题型:选择题
下列各组物质中,第一种是酸,第二种是混合物,第三种是碱的是
A.硫酸氢钠、食醋、苛性钠 B.盐酸、空气、纯碱
C.硫酸、胆矾、熟石灰 D.硝酸、食盐水、烧碱
查看答案和解析>>
科目:高中化学 来源:2016届贵州省高一上学期期中考试化学试卷(解析版) 题型:选择题
在无色透明溶液中,能够大量共存的离子组是
A.Cu2+、Na+、SO42-、OH- B.K+、Na+、HCO3-、NO3-
C.OH-、CO32--、Ca2+、Fe3+ D.Ba2+、Na+、OH-、SO42-
查看答案和解析>>
科目:高中化学 来源:2016届福建省龙岩市高一第一学期教学质量检测化学试卷(解析版) 题型:填空题
根据要求填空。
(1)下列物质中,属于电解质的是 ,属于非电解质的是 。(填序号)
①碳酸氢钠 ②CO2 ③乙醇 ④铁
(2)饮用水中的NO3-对人类健康会产生危害,为了降低饮用水中NO3-的浓度,可以在碱性条件下用铝粉将NO3-还原为N2,其化学方程式为如下:
10 Al + 6 NaNO3 + 4 NaOH +18 H2O = 10 NaAl(OH)4 + 3 N2↑
请用“单线桥法”表示上述反应中电子转移的方向和数目。
(3)已知氨气与氯气在常温条件下发生如下反应:8 NH3+3 Cl2= 6 NH4Cl +N2,该反应中还原剂与氧化剂的物质的量之比为 。
(4)今有K2SO4和Al2(SO4)3混合溶液,已知其中c(K+)= 0.2 mol·L-1,c(SO42-)= 0.7mol·L-1。则溶液中c(Al3+)= mol·L-1。
查看答案和解析>>
科目:高中化学 来源:2016届福建省龙岩市高一第一学期教学质量检测化学试卷(解析版) 题型:选择题
能正确表示下列化学反应的离子方程式是
A.饱和石灰水跟稀硝酸反应 Ca(OH)2 + 2H+ = Ca2+ + 2H2O
B.钠和水反应 Na+2H2O=Na++H2↑+2OH-
C.大理石与盐酸反应 CaCO3+2H+=Ca2++H2O+CO2↑
D.硫酸与氢氧化钡溶液反应 Ba2++OH-+H++SO42-= BaSO4↓+ H2O
查看答案和解析>>
科目:高中化学 来源:2016届福建省宁德市高一上学期期末考试化学试卷(A)(解析版) 题型:选择题
在无色的强酸性溶液中能大量共存的是
A.Mg2+、Na+、Cl-、SO42- B.K+、 Na+、 Cl-、 Cu2+
C.K+ 、Na+、NO3-、CO32- D.Na+、Ba2+、OH-、SO42-
查看答案和解析>>
科目:高中化学 来源:2016届福建省厦门市高一上学期期末质量检测模拟化学试卷(解析版) 题型:选择题
下列离子方程式的书写正确的是( )
A.实验室用大理石和稀盐酸制取CO2:2H+ + CO32- = CO2? + H2O
B.铁和稀硫酸反应:Fe + 2H+ = H2? + Fe3+
C.NH4HCO3溶液中加入过量的NaOH溶液:NH4+ + OH- = NH3+H2O
D.NaHCO3溶液与NaOH溶液反应:OH- + HCO3- = CO32- + H2O
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com