
能源是制约国家发展进程的因素之一。甲醇、二甲醚等被称为2 1世纪的绿色能源,工业上利用天然气为主要原料与二氧化碳、水蒸气在一定条件下制备合成气(CO、H2),再制成甲醇、二甲醚。
(1)工业上,可以分离合成气中的氢气,用于合成氨,常用醋酸二氨合亚铜
[Cu(NH3)2Ac]溶液(Ac=CH3COO-)(来吸收合成气中的一氧化碳,其反虚原理为:
[Cu(NH3)2Ac](aq)+CO+NH3 [Cu(NH3)3]Ac•CO(aq)(△H<0)
[Cu(NH3)3]Ac•CO(aq)(△H<0)
常压下,将吸收一氧化碳的溶液处理重新获得[Cu(NH3)2]AC溶液的措施是 ;
(2)工业上一般采用下列两种反应合成甲醇:
反应a:CO2(g)+3H2(g) CH3OH(g)+H2O(g) △H=-49.0kJ/mol
CH3OH(g)+H2O(g) △H=-49.0kJ/mol
反应b:CO(g)+2H2(g) CH3OH(g) △H<0
CH3OH(g) △H<0
①对于反应a,某温度下,将4.0 mol CO2(g)和12.0 mol H2(g)充入容积为2L的密闭容器中,反应到达平衡时,测得甲醇蒸气的体积分数为30%,则该温度下反应的平衡常数为 ;
②对于反应b,某温度下,将1.0mol CO(g)和2.0 mol H2(曲充入固定容积的密闭容器中,反应到达平衡时,改变温度和压强,平衡体系中CH3OH的物质的量分数变化情况如图所示,温度和压强的关系判断正确的是 ;(填字母代号)

A.p3>p2,T3>T2
B.p2>p4,T4>T2
C.p1>p3,T1>T3
D.p1>p4,T2>T3
(3)CO可以合成二甲醚,二甲醚可以作为燃料电池的原料,化学反应原理为:
CO(g)+4H2(g) CH3OCH3(g)+H2O(g) △H<0
CH3OCH3(g)+H2O(g) △H<0
①在恒容密闭容器里按体积比为1:4充入一氧化碳和氢气,一定条件下反应达到平衡状态。当改变反应的某一个条件后,下列变化能说明平衡一定向正反应方向移动的是 ;
A.逆反应速率先增大后减小
B.正反应速率先增大后减小
C.反应物的体积百分含量减小
D.化学平衡常数K值增大
②写出二甲醚碱性燃料电池的负极电极反应式 ;
③己知参与电极反应的电极材料单位质量放出电能的大小称为该电池的比能量。关于二甲醚碱性燃料电池与乙醇碱性燃料电池,下列说法正确的是 (填字母)
A.两种燃料互为同分异构体,分子式和摩尔质量相同,比能量相同
B.两种燃料所含共价键数目相同,断键时所需能量相同,比能量相同
C.两种燃料所含共价键类型不同,断键时所需能量不同,比能量不同
(4)已知l g二甲醚气体完全燃烧生成稳定的氧化物放出的热量为31.63 kJ,请写出表示二甲醚燃烧热的热化学方程式 。
(1)加热(2分)
(2)①1.33或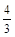 (2分,若书写单位且正确得2分,单位错误不得分) ②C、D(2分)
(2分,若书写单位且正确得2分,单位错误不得分) ②C、D(2分)
②C、D(2分)
(3)①B、D (2分)
②CH3OCH3-12e-+16OH-= 2CO32-+11H2O (2分) ③C(2分)
(4)CH3OCH3(g)+3O2(g) = 2CO2(g)+3H2O(l) ΔH=-1454.98 kJ/mol(2分)
【解析】
试题分析:(1)将吸收一氧化碳的溶液处理重新获得[Cu(NH3)2]AC溶液只要使平衡向逆反应方向移动即可,逆反应方向为气体体积增大的吸热反应,所以在高温低压下使平衡逆移。
(2)①根据反应方程式计算,
CO2(g)+3H2(g)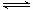 CH3OH(g)+H2O(g)
CH3OH(g)+H2O(g)
起始:4.0 mol 12.0 mol 0 0
转化:xmol 3xmol xmol xmol
平衡:4-xmol 12-xmol xmol xmol
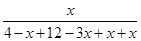 =30% x=3mol
=30% x=3mol
CO2(g)+3H2(g)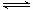 CH3OH(g)+H2O(g)
CH3OH(g)+H2O(g)
平衡浓度:0.5mol/L 1.5mol/L 1.5mol/L 1.5mol/L
t1时达到达到平衡状态,平衡常数=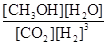 =
= =1.33或
=1.33或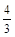
②根据化学平衡移动的影响因素:温度、压强来分析:升高温度,化学平衡向着吸热方向进行,升高压强,化学平衡向着气体体积减小的方向进行。 CH3OH的物质的量分数时随着p1、p2、p3、p4逐渐降低,说明向着逆向移动,逆向是气体体积增大的方向,所以p1、p2、p3、p4压强逐渐升高, B错,CH3OH的物质的量分数时随着T1、T2、T3、T4逐渐升高,说明正向移动,正向是放热反应,说明T1、T2、T3、T4 温度逐渐降低。A错。所以选C、D。
(3)①A.逆反应速率先增大后减小,说明一定逆向移动。
B.正反应速率先增大后减小,说明一定正向移动
C.反应物的体积百分含量减小,不一定正向移动
D.化学平衡常数K值增大,因为这个反应征方向是放热反应,说明一定正向移动
所以选B、D
②反应本质是二甲醚的燃烧,原电池负极发生氧化反应,二甲醚在负极放电,碱性环境中生成碳酸钾与氢水.正极反应还原反应,氧气在正极放电生成氢氧根离子;正极反应为氧气得到电子发生还原反应,在碱性环境中生成氢氧根离子,正极反应为3O2+12e-+6H2O=12OH-;负极上是燃料甲醚发生失电子的氧化反应,在碱性环境下,即为:CH3OCH3-12e-+16OH-= 2CO32-+11H2O ;
③由乙醇和二甲醚的分子结构可知,化学式都是C2H6O,组成元素及其原子个数完全相同,互为同分异构体,分子式和摩尔质量相同,乙醇和二甲醚的分子结构不同,无论是物理性质还是化学性质,还是共价键类型,断键时所需能量不可能完全相同,所以比能量肯定不同。所以选C(2分)
(4)l g二甲醚气体完全燃烧生成稳定的氧化物放出的热量为31.63 kJ,l mol(46g)二甲醚气体完全燃烧生成稳定的氧化物放出的热量为31.63×46= 1454.98 kJ,所以二甲醚燃烧热的热化学方程式CH3OCH3(g)+3O2(g) = 2CO2(g)+3H2O(l) ΔH=-1454.98 kJ/mol。
考点:考查涉及化学平衡移动、热化学方程式、平衡常数、原电池等内容。


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:阅读理解
 能源是制约国家发展进程的因素之一.甲醇、二甲醚等被称为2 1世纪的绿色能源,工业上利用天然气为主要原料与二氧化碳、水蒸气在一定条件下制备合成气(CO、H2),再制成甲醇、二甲醚.
能源是制约国家发展进程的因素之一.甲醇、二甲醚等被称为2 1世纪的绿色能源,工业上利用天然气为主要原料与二氧化碳、水蒸气在一定条件下制备合成气(CO、H2),再制成甲醇、二甲醚.查看答案和解析>>
科目:高中化学 来源: 题型:
(1)为了降低汽车尾气对大气的污染,有关部门拟用甲醇替代液化石油气作为公交车的燃料。已知:在25 ℃、101 kPa下,1 g甲醇燃烧生成CO2和液态水时放热22.68 kJ。请写出表示甲醇燃烧的热化学方程式。
(2)测定工业甲醇中CH3OH的质量分数可按下法:取0.100 0 g工业甲醇样品,以适量H2SO4酸化后,加入20.00 mL 0.200 0 mol·L-1的K2Cr2O7溶液,过量的K2Cr2O7溶液,再用0.300 0 mol·L-1 (NH4)2Fe(SO4)2标准溶液滴定,耗去此标准液20.00 mL时,刚好到达滴定终点。
已知:CH3OH+![]() +8H+
+8H+![]() CO2↑+2Cr3++6H2O
CO2↑+2Cr3++6H2O
①写出H2SO4酸化的K2Cr2O7溶液与(NH4)2Fe(SO4)2溶液反应的离子方程式。
②求此工业甲醇中CH3OH的质量分数。
查看答案和解析>>
科目:高中化学 来源: 题型:
能源是人类社会发展进步的物质基础,能源、信息、材料一起构成了现代文明的三大支柱。甲醇(CH3OH)是一种重要的化工原料,广泛应用于化工生产,也可以直接用做燃料,并且能显著降低汽车尾气对大气的污染。
Ⅰ.请写出甲醇的电子式_ __;与甲醇的物质的量相同的某有机物,完全燃烧时消耗的氧气的量也与甲醇相同,写出符合上述条件的任一有机物的化学式__ __。
Ⅱ.已知CH30H(1)+O2 (g)=CO(g)+2H2O(g) ![]()
2CO(g)+O2 (g)=2CO2 (g) ![]()
(1)试写出CH3OH(1)完全燃烧[生成H2O(g)]的热化学方程式:
(2)有人建议,投资研究由CO2和H2O(g)来制取CH3OH(1),如果成功,既能缓解能源紧张,又能解决温室效应的问题。请你分析论证,该建议是否可行?
Ⅲ.(1)以甲醇溶液、氧气为基本反应物的新型燃料电池已经问世,其结构如图所示(甲醇解离产生的H+可以通过质子交换膜进入另一极)。请写出甲醇在电极上反应的方程式:________, 当有32g甲醇被完全氧化时,转移电子____mo1。
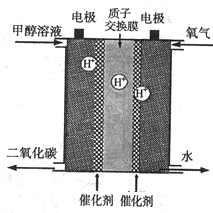
(2)某同学以甲醇燃料电池为电源,均以石墨为电极电解CuSO4溶液,则与电源正极相连的电解池电极上的电极反应式为____
查看答案和解析>>
科目:高中化学 来源: 题型:
能源是人类社会发展进步的物质基础,在当代,能源、信息、材料一起构成了现代文明的三大支柱。为了缓解能源危机和减少汽油燃烧所产生的污染,目前已普遍推广使用新型车用燃烧――乙醇汽油。乙醇汽油是将乙醇和普通汽油按一定体积比混合而成的,已知某乙醇汽油蒸气中乙醇和汽油的体积比约为1:4。请回答下列问题:
(1)若以辛烷代表汽油的成分,请写出乙醇汽油燃烧的化学方程式:
。
(2)若以辛烷代表汽油的成分,并设空气中氧气所占的体积分数为![]() ,则相同条件下,相同体积汽油、乙醇汽油分别在气缸内完全燃烧时,所消耗空气的体积比是 。
,则相同条件下,相同体积汽油、乙醇汽油分别在气缸内完全燃烧时,所消耗空气的体积比是 。
(3)若用乙醇汽油设计燃料电池,在一个电极通入空气,另一个电极通入乙醇汽油蒸气,电解质是掺杂了Y2O3的ZrO2晶体,它在高温下能传导O2-,则该电极正极发生的电极反应是 。
(4)据最新报道,巴西新一代乙醇燃料汽车总量已突破200万辆,为了更好推广乙醇燃料汽车的使用,巴西政府决定向普通汽车购买者征收16%的消费税,而只向乙醇燃料汽车购买者征收14%的消费税。巴西地处南美洲,是世界上甘蔗产量巨大的国家之一,乙醇是从甘蔗中提炼中加工出来的。请写出由甘蔗渣制备乙醇的化学反应方程式 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com