
| A. | CaCO3$\frac{\underline{\;高温\;}}{\;}$CaO+CO2↑ | B. | Na2O+H2O═2NaOH | ||
| C. | 4HNO3(浓)$\frac{\underline{\;\;△\;\;}}{\;}$4NO2↑+O2↑+2H2O | D. | Na2CO3+2HCl═2NaCl+H2O+CO2↑ |
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

 ;
; +3NaOH $→_{高压}^{高温}$
+3NaOH $→_{高压}^{高温}$ +NaCl+2H2O;
+NaCl+2H2O; ;
; (任写一种结构简式).
(任写一种结构简式).查看答案和解析>>
科目:高中化学 来源: 题型:解答题
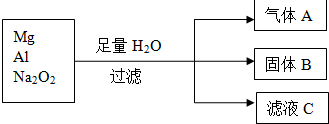
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 按系统命名法,有机物 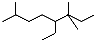 可命名为3,3,7-三甲基-4-乙基辛烷 可命名为3,3,7-三甲基-4-乙基辛烷 | |
| B. | 石油制乙烯、煤的液化、蛋白质的盐析、肥皂去油污均涉及化学变化 | |
| C. | 等质量的乙醇与乙烯完全燃烧,前者生成更多的水 | |
| D. | 全降解塑料 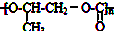 可由环氧丙烷( 可由环氧丙烷(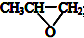 )和CO2反应制得 )和CO2反应制得 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
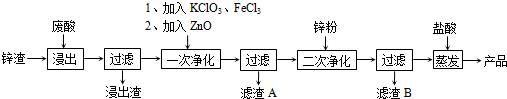
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
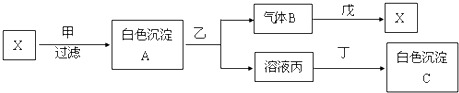
 ;
;查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | n=5 | B. | n<5 | C. | n>5 | D. | 无法判断 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com