
(10分)氧化还原反应在生产、生活中应用广泛,酸性KMnO4、H2O2、Fe(NO3)3是重要的氧化剂.用所学知识回答问题:
(1)3H2SO4+2 KMnO4+5H2O2=K2SO4+2MnSO4+5 O2↑+8 H2O,当有6 mol H2SO4参加反应的过程中,有 mol还原剂被氧化。
(2)在稀硫酸中,KMnO4能将H2C2O4氧化为CO2。该反应的化学方程式为 。
(3)取300mL 0.2mol/L的KI溶液与一定量的酸性KMnO4溶液恰好反应,生成等物质的量的I2和KIO3,则消耗KMnO4的物质的量的是 mol。
(4)在Fe(NO3)3溶液中加入Na2SO3溶液,溶液先由棕黄色变为浅绿色,过一会又变为棕黄色,溶液先变为浅绿色的离子方程式是 ,又变为棕黄色的原因是 。
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源:2016届云南省高三第一次月考试卷化学试卷(解析版) 题型:选择题
二甘醇可用作溶剂、纺织助剂等。它一旦进入人体会导致急性肾衰竭,危及生命。其结构简式是HO—CH2CH2—O—CH2CH2—OH,下列有关二甘醇的叙述正确的是
A.不能发生酯化反应 B.能发生取代反应
C.能溶于水,不溶于乙醇 D.符合通式CnH2nO3
查看答案和解析>>
科目:高中化学 来源:2015-2016学年辽宁省高二上化学试卷(解析版) 题型:选择题
下列对非金属元素(除稀有气体元素外)的相关判断正确的是
①非金属元素都是主族元素
②单质在反应中都只能作氧化剂
③氢化物常温下都是气态,所以都叫气态氢化物
④氧化物常温下都可以与水反应生成酸
⑤非金属元素R所形成的含氧酸盐(MaROb)中的R元素必定呈现正价
A.②⑤ B.①③⑤ C.②③④ D.①⑤
查看答案和解析>>
科目:高中化学 来源:2015-2016学年北大附中河南分校高二上9月考化学试卷(解析版) 题型:选择题
在298K、100kPa时,已知:2H2O(g)=O2(g)+2H2(g)△H1
Cl2(g)+H2(g)=2HCl(g )△H2
2Cl2(g)+2H2O(g)=4HCl(g)+O2(g)△H3
则△H3与△H1和△H2间的关系正确的是
A.△H3=△H1+2△H2 B.△H3=△H1+△H2
C.△H3=△H1﹣2△H2 D.△H3=△H1﹣△H2
查看答案和解析>>
科目:高中化学 来源:2016届四川省高三上学期第一次月考化学试卷(解析版) 题型:选择题
下列叙述错误的是
A.常温下,将pH=11的氨水和pH=3的盐酸等体积混合后,所得溶液中各离子浓度的关系是c(NH4+)>c(Cl-)>c(OH-)>c(H+)
B.在BaSO4饱和溶液中加入少量的BaCl2溶液产生沉淀,平衡后的溶液中:
(Ba2+)×c(SO42-)>Ksp(BaSO4);c(Ba2+)>c(SO42-)
C.某二元酸的电离方程式为H2B=H++HB-,HB- H++B2-,所以NaHB溶液呈酸性
H++B2-,所以NaHB溶液呈酸性
D.等浓度的NH4HSO4、NH4Cl、NH3.H2O溶液中c(NH4+)逐渐减小
查看答案和解析>>
科目:高中化学 来源:2016届山西省忻州市高三上学期第一次月考化学试卷(解析版) 题型:选择题
分第枝酸可用于生化研究,其结构简式如图。下列关于分枝酸的叙述正确的是
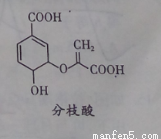
A.在与氢气加成时最多消耗5molH2
B.可与乙醇、乙酸反应,且反应类型相同
C.1mol分枝酸最多可与3molNaOH发生中和反应
D.可使溴的四氯化碳溶液、酸性高锰酸钾溶液褪色,且原理相同
查看答案和解析>>
科目:高中化学 来源:2016届山东省高三上学期一模化学试卷(解析版) 题型:选择题
将0.02 molNa分别投入到盛有100 mL水、100 mL 1mol·L-1盐酸、100 mL 1mol·L-1硫酸铜溶液的X、Y、Z三个烧杯中,下列有关说法错误的是
A.三个烧杯中一定均会发生的离子反应有:2Na+2H2O=2Na++2OH-+H2↑
B.三个烧杯中钠均在液面上剧烈反应,相比而言,X烧杯中的反应平缓些
C.Z烧杯中一定会有沉淀生成,但沉淀不是单质铜
D.三个烧杯中生成氢气的物质的量相同
查看答案和解析>>
科目:高中化学 来源:2015-2016学年山西省太原市高一上入学考试化学试卷(解析版) 题型:选择题
鉴别下列各组物质所用的试剂或方法不正确的是( )
A、硬水、软水(肥皂水)
B、稀盐酸、食盐水(酚酞试液)
C、涤纶、羊毛制品(点燃)
D、空气、氧气(带火星的木条)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com