
| A. | 加入氯水后振荡,看水层里是否有棕红色的溴出现 | |
| B. | 加入硝酸银溶液,再加稀硝酸,观察有无浅黄色沉淀生成 | |
| C. | 加入NaOH水溶液共热,冷却后加硝酸银溶液,观察有无浅黄色沉淀生成 | |
| D. | 加入NaOH水溶液共热,冷却后用过量稀硝酸中和过量碱后,再加硝酸银溶液,观察有无浅黄色沉淀生成 |
 夺冠金卷全能练考系列答案
夺冠金卷全能练考系列答案科目:高中化学 来源: 题型:解答题
 运用元素周期律研究元素及其化合物的性质具有重要意义.
运用元素周期律研究元素及其化合物的性质具有重要意义.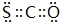 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 蛋白质、淀粉、纤维素、葡萄糖等都能在人体内水解并提供能量 | |
| B. | 将甲烷和乙烯的混合气体通过盛有溴水的洗气瓶,即可提纯甲烷 | |
| C. | C2H6与氯气发生取代反应,C2H4与HCl发生加成反应,均可得到C2H5Cl | |
| D. | 用溴水一种试剂就可将苯、CCl4、乙酸、乙醇区别 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
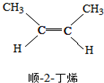 ?
? △H=-4.2kJ/mol.
△H=-4.2kJ/mol.| A. | 顺-2-丁烯比反-2-丁烯稳定 | |
| B. | 顺-2-丁烯的燃烧热比反-2-丁烯大 | |
| C. | 降温有利于平衡向生成顺-2-丁烯反应方向移动 | |
| D. | 反-2-丁烯和顺-2-丁烯具有相同的熔沸点 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 改变汽车尾气排放压强 | |
| B. | 提高反应温度 | |
| C. | 在尾气排放处使用催化剂 | |
| D. | 向汽车发动机燃烧室中通入过量的空气 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | I-131:${\;}_{19}^{39}X$ | B. | Cl-的结构示意图: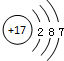 | ||
| C. | 强电解质:BaSO4 | D. | 碱性氧化物:Na2O2 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | X>Y | B. | W>Z | C. | Z>Y | D. | Z>X |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 碳酸钙与盐酸反应:CO32-+2H+═CO2↑+H2O | |
| B. | 铜和硝酸银溶液反应:Cu+Ag+═Cu2++Ag | |
| C. | 铁与氯化铁溶液反应:Fe+2Fe3+═3Fe2+ | |
| D. | 氢氧化钡溶液与硫酸反应:Ba2++OH-+H++SO42-═BaSO4↓+H2O |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com