
 H
H H,则
H,则 H= ;
H= ;
 请在答题卡上写出并配平反应式(a);
请在答题卡上写出并配平反应式(a);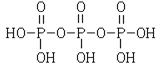 (2分) ,Na5P3O10(2分)
(2分) ,Na5P3O10(2分) 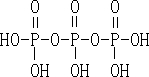 ;“五钠”即五个钠原子,所以三聚磷酸钠的化学式为Na5P3O10。
;“五钠”即五个钠原子,所以三聚磷酸钠的化学式为Na5P3O10。

科目:高中化学 来源:不详 题型:单选题
 C(g)+D(g)过程中的能量变化如图所示,由此可判断( )
C(g)+D(g)过程中的能量变化如图所示,由此可判断( )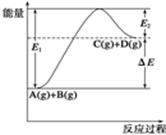
| A.1molA与1molB充分反应后,能量变化为ΔE |
| B.加入催化剂后,反应加快,ΔE减小 |
| C.反应物的总键能小于生成物的总键能 |
| D.反应达到平衡时,升高温度,A的转化率增大 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
 R(g) △H = -Q1 kJ·mol-1,②2R (g)+N(g)
R(g) △H = -Q1 kJ·mol-1,②2R (g)+N(g) 2T (g) △H = -Q2 kJ·mol-1。 Q1、Q2、Q3均为正值。下列说法正确的是
2T (g) △H = -Q2 kJ·mol-1。 Q1、Q2、Q3均为正值。下列说法正确的是| A.1 mol R(g)的能量总和大于1 mol M(s)与1 mol N(g) 的能量总和 |
| B.将2 mol R (g)与1 mol N(g)在该条件下充分反应,放出热量Q2 kJ |
C.当1 mol M(s)完全转化为T (g)时(假定无热量损失),放出热量Q1+ kJ kJ |
D.M(g)+N(g) R(g) △H=-Q3 kJ·mol-1 , 则Q3<Q1 R(g) △H=-Q3 kJ·mol-1 , 则Q3<Q1 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题

查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
 2NH3(g)(放热反应)。下列描述中正确的是
2NH3(g)(放热反应)。下列描述中正确的是| A.N2和H2具有的总能量一定比NH3具有的总能量低 |
| B.a、b、c三者的关系为:a+3b<2c |
| C.向密闭容器中通入1molN2和3molH2,反应放出的热量必为(6c―a―3b)kJ |
| D.形成1molN—H会放出ckJ热量 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.等物质的量的CH4参加反应,反应①②转移的电子数相同 |
| B.CH4(g)+4NO2(g)=4NO(g)+CO2(g)+2H2O(g)△H=-530 kJ/mol |
| C.0.2 mol CH4还原NO2至N2,且生成H2O(g)放出的热量为164.6 kJ |
| D.若用4.48 L(标准状况)CH4还原NO2至N2且生成H2O(g),整个过程中转移电子1.60 mol |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题



 其相关数据如下表所示:
其相关数据如下表所示:

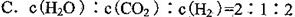

查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
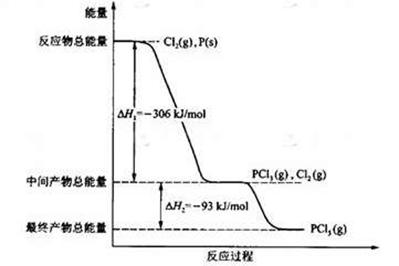
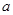 1等于 ;若反应温度由T1升高到T2,平衡时PCl5的分解率为
1等于 ;若反应温度由T1升高到T2,平衡时PCl5的分解率为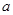 2,
2,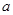 2
2 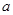 1(填“大于”、“小于”或“等于”);
1(填“大于”、“小于”或“等于”);查看答案和解析>>
科目:高中化学 来源:不详 题型:问答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com