
| A. | 相同条件下,电离平衡常数越小,表示弱电解质的电离能力越弱 | |
| B. | 相同条件下,化学平衡常数越大,表示该反应的反应速率越大 | |
| C. | 其它条件不变时,升高温度,化学平衡常数一定增大 | |
| D. | 多元弱酸各步电离平衡常数相互关系为K1<K2<K3 |
分析 A.电离平衡常数(K)是温度的常数,随温度的增大而增大,不随浓度的变化而变化;相同条件下K越大,酸的电离程度越大;
B.相同条件下,化学平衡常数越大,反应速率不一定大;
C.化学平衡常数随温度变化,温度发生变化时,平衡常数和反应的吸热或放热方向有关,升温向吸热反应方向进行;
D.多元弱酸各步电离平衡常数依次减小,据此分析.
解答 解:A、相同条件下K越大,酸的电离程度越大,所以相同条件下,电离平衡常数越小,表示弱电解质的电离能力越弱,故A正确;
B、化学平衡常数是衡量反应进行程度的物理量,和反应速率无直接关系,故B错误;
C、正反应是吸热反应的化学平衡,升温平衡正向进行,平衡常数增大,但正反应为放热反应的化学平衡,升温平衡逆向进行,平衡常数减小,故C错误;
D、多元弱酸分步电离,电离程度依次减小,所以多元弱酸各步电离平衡常数相互关系为K1>K2>K3,故D错误;
故选A.
点评 本题考查了电离平衡常数、化学平衡常数的理解应用,注意平衡常数(K)是温度的常数,题目难度中等.


科目:高中化学 来源: 题型:选择题
| 编号 性质 | ① | ② | ③ | ④ | ⑤ | ⑥ | ⑦ | ⑧ | |
| 原子半径(10-10m) | 0.74 | 1.60 | 1.52 | 1.10 | 0.99 | 1.86 | 0.75 | 0.89 | |
| 主 要 化 合 价 | 最高价 | +2 | +1 | +5 | +7 | +1 | +5 | +2 | |
| 最低价 | -2 | -3 | -1 | -3 | |||||
| A. | ③和⑥、④和⑦分别处于同一主族 | |
| B. | 元素④处于第3周期ⅤA族 | |
| C. | 元素⑥对应的氢氧化物是强碱 | |
| D. | 元素①与元素⑥形成的化合物中不可能存在共价键 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
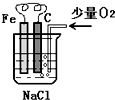 分析图,按要求写出有关反应方程式:
分析图,按要求写出有关反应方程式:查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| CaSO4 | CaCO3 | BaSO4 | BaCO3 |
| 2.6×10-2 | 7.8×10-4 | 2.4×10-4 | 1.7×10-3 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 推广燃煤脱硫技术,减少SO2污染,同时把煤粉碎了再燃烧以提高煤的燃烧效率 | |
| B. | 开发太阳能、风能和氢能等能源代替化石燃料,有利于节约资源、保护环境 | |
| C. | 采用“绿色化学”工艺,使原料尽可能转化为所需要的物质 | |
| D. | 在汽车尾气处理器中使用新的催化剂,促使平衡2CO+2NO?2CO2+N2向正反应方向移动,减少污染物的排放 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 0.1 mol羟基中含有的电子数为0.9 NA | |
| B. | 标准状况下,12g金刚石中含共价键的数目为4NA | |
| C. | 0.1 mol N2与足量H2充分反应,转移的电子数为0.6 NA | |
| D. | 235g核素92235U发生裂变反应:92235U+01n$\stackrel{裂变}{→}$2890Sr+54136Xe+1001n净产生的中子(01n)数为10NA |
查看答案和解析>>
科目:高中化学 来源: 题型:计算题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com