
| A.OH一、F—、O2—、Ne | B.CH4、NH3、H2O、HF |
| C.NH4+、Na+、H3O+、PH4+ | D.F一、O2一、Mg2+、A13+ |
 全能测控期末小状元系列答案
全能测控期末小状元系列答案科目:高中化学 来源:不详 题型:填空题

 A+L的化学方程式为: 。
A+L的化学方程式为: 。 。
。 。
。查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题

查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
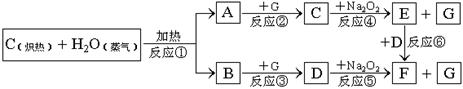
 ;E
;E  。(NA表示阿佛加德罗常数)
。(NA表示阿佛加德罗常数) ol。
ol。查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.NO和O2+ | B.CO和NO | C.NO2和CO2 | D.SO2和ClO2 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.H原子变成He原子属于化学变化,不属于物理变化 |
| B.He原子半径大于H半径 |
| C.在一定条件下质量可转变成能量 |
| D.在遥远的将来(约50亿年后)太阳会“烧尽” |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题



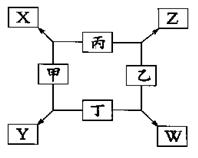



查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com