
下列关于化石燃料的说法正确的是
A.石油分馏可获得石油气、汽油、苯及其同系物等
B.石油催化裂化主要得到乙烯、乙炔等
C.煤含有苯和甲苯,可干馏后获得苯和甲苯
D.煤的液化、气化属于均属于化学变化
科目:高中化学 来源:2014-2015黑龙江省鸡西市龙东南七校高一上学期期末联考化学试卷(解析版) 题型:选择题
用特殊的方法把固体物质加工到纳米级的超细粉末粒子,然后制得纳米材料。下列分散系中分散质的微粒直径和这种粒子具有相同数量级的是
A.溶液 B.悬浊液 C.胶体 D.乳浊液
查看答案和解析>>
科目:高中化学 来源:2014-2015黑龙江省高二上学期期末考试化学试卷(解析版) 题型:选择题
在给定的溶液中加入以下各种离子,各离子能大量共存的是
A.滴加甲基橙试液显红色的溶液:Fe3+、NH4+、Cl-、SCN-
B.pH=1的溶液: Cu2+、Na+、Mg2+、NO3-
C.水电离出来的c(H+)=10-13mol/L的溶液:K+、HCO3-、Br-、Ba2+
D.所含溶质为Na2SO4的溶液:K+、CO32-、NO3-、Al3+
查看答案和解析>>
科目:高中化学 来源:2014-2015学年上海市十三校高三第二次联考化学试卷(解析版) 题型:选择题
工业上以铬铁矿(主要成分为FeO·Cr2O3)、碳酸钠、氧气、和硫酸为原料生产重铬酸钠(Na2Cr2O7·2H2O),其主要反应为:
(1)4FeO·Cr2O3 + 8Na2CO3 + 7O2 8Na2CrO4 + 2Fe2O3 + 8CO2
8Na2CrO4 + 2Fe2O3 + 8CO2
(2)2Na2CrO4 + H2SO4→Na2SO4 + Na2Cr2O7 + H2O
下列说法正确的是
A.反应(1)和(2)均为氧化还原反应
B.反应(1)的氧化剂是O2,还原剂是FeO·Cr2O3
C.高温下,O2的氧化性强于Fe2O3,弱于Na2CrO4
D.反应(1)中每生成1molNa2CrO4时电子转移3mol
查看答案和解析>>
科目:高中化学 来源:2014-2015学年上海市十三校高三第二次联考化学试卷(解析版) 题型:选择题
工业上制备下列金属,采用的化学反应原理正确的是
A.镁:2MgO (熔融)  Mg+O2↑ B.钙:CaO+C
Mg+O2↑ B.钙:CaO+C Ca+CO↑
Ca+CO↑
C.锰:3MnO2+4Al 3Mn+2Al2O3 D.汞:HgS
3Mn+2Al2O3 D.汞:HgS Hg+S
Hg+S
查看答案和解析>>
科目:高中化学 来源:2014-2015学年北京市顺义区高三第一次统一练习化学试卷(解析版) 题型:填空题
(12分)工业上采用下列工艺流程将石油废气中的硫化氢转化为硫酸和氢气等产品以防止污染。
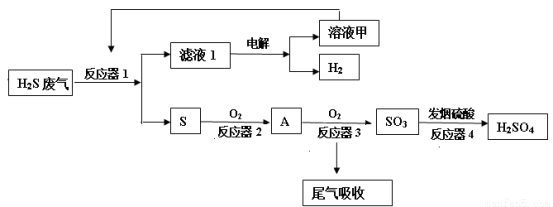
(1)反应器1中装有硫酸铁的酸性溶液。
①配制硫酸铁溶液时,需加入适量的硫酸,请用化学平衡移动原理解释原因 。
②反应器1中发生反应的离子方程式是______.
(2)反应器3中发生反应的化学方程式是 。
(3)工业上用氨水和热空气吸收处理尾气中的二氧化硫以生产氮肥,该反应的化学方程式是______.
(4)电解滤液1的工作原理示意图如下:
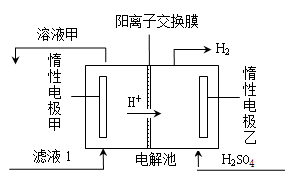
①乙电极是 (填“阴”或“阳”)极。
②甲电极的电极反应式是 。
③电解滤液1的离子方程式是 。
查看答案和解析>>
科目:高中化学 来源:2014-2015学年北京市顺义区高三第一次统一练习化学试卷(解析版) 题型:选择题
25℃时,在浓度均为1 mol/L的溶液中,各组离子一定能大量共存的是
A.盐酸中:K+、Mg2+、Fe2+、MnO7-、
B.NaOH溶液中:Cu2+、NH4+、SO42-、CO32-
C.FeCl3溶液中:Al3+、Na+、SCN-、SO42-
D.NaClO溶液中:K+、SO42-、OH-、NO3-
查看答案和解析>>
科目:高中化学 来源:2014-2015学年江苏省扬州市高三上学期期末考试化学试卷(解析版) 题型:选择题
25℃时,下列有关溶液中微粒的物质的量浓度关系正确的是
A.在0.1 mol·L-1 NH4Cl溶液中:c(H+)=c(NH3·H2O)+c(OH-)
B.10 mL 0.1 mol·L-1 CH3COONa溶液与6 mL 0.2 mol·L-1盐酸混合:c(Cl-) > c(Na+) > c(OH-) > c(H+)
C.0.1 mol·L-1 NH4HSO4溶液与0.1 mol·L-1 NaOH溶液等体积混合:c(Na+) = c(NH4+) > c(H+) > c(OH-)
D.0.1 mol·L-1 HCN溶液和0.05 mol·L-1 NaOH溶液等体积混合(pH>7):c(HCN) + c(H+) > c(OH-) + c(CN-)
查看答案和解析>>
科目:高中化学 来源:2014-2015学年湖南省长沙市高三4月月考理综化学试卷(解析版) 题型:实验题
(15分)硫代硫酸钠(Na2S2O3)俗名大苏打,可用做分析试剂。它易溶于水,难溶于酒精,受热、遇酸易分解。工业上可用硫化碱法制备,反应原理:2Na2S + Na2CO3 + 4SO2=3Na2S2O3 + CO2,实验室模拟该工业过程的装置如图所示,回答下列问题:
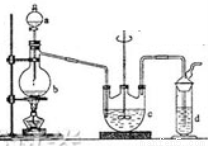
(1)b中反应的离子方程式为_________________________,c中试剂为__________。
(2)反应开始后,c中先有浑浊产生,后又变为澄清,此浑浊物是____________。
(3)控制b中的溶液的pH接近7,停止通入SO2。若未控制好,pH<7,会影响产率,原因是(用离子方程式表示) 。
(4)停止通入SO2后,将c中的溶液抽入d中,d中的试剂为________。
(5)将d所得液溶转移到蒸发皿中,水浴加热浓缩,冷却结晶、过滤、洗涤,洗涤晶体所用的试剂为(填化学式) 。
(6)实验中要控制SO2生成速率,可采取的措施有________________(写出一条)。
(7)为检验制得的产品的纯度,该实验小组称取5.0克的产品配制成250mL硫代硫酸钠溶液,并用间接碘量法标定该溶液的浓度:在锥形瓶中加入25mL0.01mol/LKIO3溶液,并加入过量的KI酸化,发生下列反应:5I-+IO3-+6H+=3I2+3H2O,再加入几滴淀粉溶液,立即用所配Na2S2O3溶液滴定,发生反应:I2+2S2O32-=2I-+S4O62-,当蓝色褪去且半分钟不变色时达到滴定终点。实验数据如下表:
实验序号 | 1 | 2 | 3 |
Na2S2O3溶液体积(mL) | 19.98 | 20.02 | 21.18 |
则该产品的纯度是 ,(用百分数表示,保留1位小数)间接碘量法滴定过程中可能造成实验结果偏低的是 。
A.滴定管未用Na2S2O3溶液润洗
B.滴定终点时仰视读数
C.锥形瓶用蒸馏水润洗
D.滴定管尖嘴处滴定前无气泡,滴定终点发现气泡
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com