
ij��ѧ��ȤС��ʵ��̽����̽��̼����Ԫ�صķǽ����Ե����ǿ��������Ҫ��ش��������⣺
��1��ʵ��װ�����£���װ��E��ʢ��������KMnO4��Һ��

��д��ʾ��������A
��2��ʵ�鲽�裺 ����������_________ ____����ҩƷ��a��Ȼ�����Ũ���ᣬ����
��3������̽������ͭ��Ũ���ᷴӦ�Ļ�ѧ����ʽ��
����˵��̼Ԫ�صķǽ����Աȹ�Ԫ�طǽ�����ǿ��ʵ��������
�������Թ�D�е�ʵ�������ܷ�֤����Ԫ�صķǽ�����ǿ��̼Ԫ�صķǽ�����
___ __����ܡ�����ԭ����
 ��������һ���þ�ϵ�д�
��������һ���þ�ϵ�д� Сѧ��10����Ӧ����ϵ�д�
Сѧ��10����Ӧ����ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
��϶�����Ԫ�ص������û�ѧ����ش��������⣺
��1����ˮ��Ӧ����ҵĽ�����_____________��д����Ӧ�����ӷ���ʽΪ_____________����2����ˮ��Ӧ����ҵķǽ���������_____________��д����Ӧ�Ļ�ѧ����ʽΪ_____________��
��3�����ȶ�����̬�⻯��Ļ�ѧʽ��_____________��
��4����ϡ�������⣬ԭ�Ӱ뾶����Ԫ����_____������ԭ�Ӱ뾶��С��Ԫ���γɵĻ��������� �����ӡ����ۣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
������ͼ��ʾװ�ÿ���ģ������ĵ绯ѧ����������˵����ȷ����
 A����XΪп��������K����M��������������ԭ��Ӧ
A����XΪп��������K����M��������������ԭ��Ӧ
B����XΪ̼��������K����N����X��������ԭ��Ӧ
C����XΪ̼��������K����N�����ɼӿ����ĸ�ʴ
D����XΪп��������K����M�����ɼӿ����ĸ�ʴ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
���¹��ڵ�IA��Ԫ�غ͵ڢ�A��Ԫ�ص��й�������ȷ����
A�����ϵ��£���IA��Ԫ�ص��ʵ��ܶ�������
B�����ϵ��£���IA��Ԫ�ص��ʵ��۵�����
C�����ϵ��£��� ��A��Ԫ�����⻯����ȶ�������ǿ
D�����ϵ��£��� ��A��Ԫ�����⻯��ķе�������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����˵����ȷ����(����)
�����������ʻ��ã�����������Ϻ�����������ը
��ʵ������ȡ����ʱ��Ϊ�˷�ֹ������Ⱦ���������������������������Һ����
��������ˮ��������ǿ�ھ�����ˮ
�ܼ���HCl�������Ƿ����Cl2�����ǽ�����ͨ����������Һ
�ݳ�ȥHCl�����е�Cl2���ɽ�����ͨ�뱥��ʳ��ˮ
A���٢ڢۡ����� B���ڢۢ� C���� D���ۢ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
��ͼ�Dz��ֶ�����Ԫ�ػ��ϼ���ԭ�������Ĺ�ϵͼ������˵����ȷ����
A��ԭ�Ӱ뾶��Z��Y��X
B����̬�⻯��Ļ�ԭ�ԣ�W��R
C��WX3��ˮ��Ӧ�γɵĻ����������ӻ�����
D����Z������Һһ����ʾ����

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�������糧�ͷų������������NOx����SO2��CO2���������ɻ������⡣��ȼú���������������������̼�ȴ�������ʵ����ɫ���������ܼ��š��������õ�Ŀ�ġ�
��1�����������ü������ԭNOx��
CH4(g) �� 4NO2(g) ��4NO(g) �� CO2(g) �� 2H2O(g) ��H1����574 kJ��mol��1
CH4(g) �� 4NO(g) ��2N2(g) �� CO2(g) �� 2H2O(g) ��H2����1160 kJ��mol��1
����ֱ�ӽ�NO2��ԭΪN2���Ȼ�ѧ����ʽΪ ��
��2����̼����CO2ת��Ϊ�״���CO2(g)��3H2(g) CH3OH(g)��H2O(g) ��H3
CH3OH(g)��H2O(g) ��H3
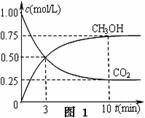
����һ���º����ܱ������г���1 mol CO2��3 mol H2����������Ӧ�����CO2��CH3OH(g)Ũ����ʱ��仯��ͼ1��ʾ���ش�0~10 min�ڣ�������ƽ����Ӧ����Ϊ
mol/(L��min)����10 min�����¶Ȳ��䣬����ܱ��������ٳ���1 mol CO2(g)��1 mol H2O(g)����ƽ�� ������������������ƶ���
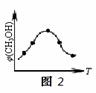
��ȡ��ݵ������CO2��H2�Ļ�����壨���ʵ���֮�Ⱦ�Ϊ1��3�����ֱ�����¶Ȳ�ͬ���ݻ���ͬ�ĺ����ܱ������У�����������Ӧ����Ӧ��ͬʱ�������ü״��������������CH3OH���뷴Ӧ�¶�T�Ĺ�ϵ������ͼ2��ʾ��������CO2ת��Ϊ�״��ķ�Ӧ�ġ�H3 0�����������������������
��3����������Na2SO3��Һ���ѳ������е�SO2��Na2SO3����NaOH��Һ����SO2�Ƶá�NaOH��Һ����SO2�Ĺ����У�pH��n(SO32-)�Un(HSO3��)�仯��ϵ���±���
| n(SO32��)�Un(HSO3��) | 91�U9 | 1�U1 | 9�U91 |
| pH | 8.2 | 7.2 | 6.2 |
�� ���ϱ��жϣ�NaHSO3��Һ���� �����ԣ� �û�ѧƽ��ԭ�����ͣ��������������������� ������
�� ����Һ������ʱ������Ũ�ȹ�ϵ��ȷ���ǣ�ѡ����ĸ��������������
a��c(Na+)=2c(SO32-)+c(HSO3-)
b��c(Na+) > c(HSO3-) > c(SO32-) > c(H+) = c(OH-)
c��c(Na+) + c(H+) = c(SO32-) + c(HSO3-) + c(OH-)
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
��֪ij��Һ�д���OH-��H+��NH4+��Cl- �������ӡ�ijͬѧ�Ʋ�������Ũ�ȴ�С˳�������¹�ϵ��
�٣�c(Cl-)>c(NH4+)>c(H+)>c(OH-) �ڣ�c(Cl-)>c(NH4+)>c(OH-)>c(H+)
�ۣ�c(NH4+)>c(Cl-)>c(OH-)>c(H+) �ܣ�c(Cl-)>c(H+)>c(NH4+)>c(OH-)
��д���пհף�
��1������Һ��ֻ�ܽ���һ�����ʣ����������_____________________���ѧʽ��������������Ũ�ȵĴ�С��ϵΪ_____________������ţ�
��2����������ϵ�Т�����ȷ�ģ�����Һ�е�����Ϊ_____________________���ѧʽ��
��3��������Һ���������ȵ�ϡ����Ͱ�ˮ��϶��ɣ�ǡ�ó����ԣ�����ǰc(HCl)________c(NH3��H2O)������ڡ���С�ڡ����ڡ�����ͬ�������ǰ����c(H+)�ͼ���c(OH-)�Ĺ�ϵΪc(H+)______________c(OH-)
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
��֪X��Y��Z��W��Ϊ��ѧ��ѧ�г����ĵ��ʻ������֮���ת����ϵ��ͼ��ʾ(���ֲ�������ȥ)����W��X��������(����)

| ѡ�� | W | X |
| A | ���� | Na2CO3��Һ |
| B | ϡHNO3 | Fe |
| C | CO2 | Ca(OH)2��Һ |
| D | O2 | Na |
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com