
正确掌握化学用语和化学基本概念是学好化学的基础。下列有关表述中正确的一组是
A.过氧乙酸(CH3COOOH)与羟基乙酸(HOCH2COOH)互为同分异构体; 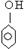 与
与  互为同系物
互为同系物
B.金刚石、CH4、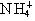 粒子的空间构型均为正四面体;晶体硅、碳化硅均为原子晶体
粒子的空间构型均为正四面体;晶体硅、碳化硅均为原子晶体
C.16O与18O互为同位素;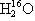 、
、 、
、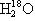 、
、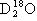 互为同素异形体
互为同素异形体
D.Ca2+的结构示意图为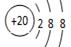 ,NH4CI的电子式为
,NH4CI的电子式为
科目:高中化学 来源: 题型:
下列事实能说明乙酸(CH3COOH) 属于弱酸的是 ( )
① 1mol/L CH3COOH的 pH=2 ②乙酸能与水以任意比互溶
③ 20mL 1mol/L CH3COOH 与20mL 1mol/LNaOH恰好中和
④ CH3COONa溶液的pH>7
A.①② B.②③ C.③④ D.①④
查看答案和解析>>
科目:高中化学 来源: 题型:
化学科学需要借助化学专用语言来描述,现有下列化学用语:①Cl-的结构示意图:
 ;②羟基的电子式:
;②羟基的电子式: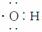 ;③HClO的结构式:H—Cl—O;④NaHCO3在水中的电离方程式:NaHCO3===Na++H++CO
;③HClO的结构式:H—Cl—O;④NaHCO3在水中的电离方程式:NaHCO3===Na++H++CO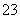 ;⑤碳酸氢铵与足量的氢氧化钠溶液混合:HCO
;⑤碳酸氢铵与足量的氢氧化钠溶液混合:HCO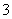 +OH-===CO
+OH-===CO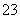 +H2O;⑥CO2的比例模型:
+H2O;⑥CO2的比例模型: ;⑦原子核内有10个中子的氧原子:
;⑦原子核内有10个中子的氧原子: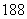 O。其中说法正确的是 ( )
O。其中说法正确的是 ( )
A.①②⑦ B.④⑤⑥
C.②③④⑥ D.②③⑤⑥⑦
查看答案和解析>>
科目:高中化学 来源: 题型:
化学用语是学习化学的重要工具,下列用来表示物质变化的化学用语中,正确的是
A .钢铁腐蚀时可能发生的反应(正极):2H2O+O2-4e-=4OH-
.钢铁腐蚀时可能发生的反应(正极):2H2O+O2-4e-=4OH-
B.1 L、0.5 mol/L稀硫酸与1 L、1 mol/LNaOH溶液反应放出57.3kJ的热,则其中和热的热化学方程式:H2SO4(aq)+2NaOH(aq)=Na2SO4(aq)+2H2O(l);△H= -114.6 kJ/mol
C.碳酸氢钠溶液与足量澄清石灰水反应:HCO3-+Ca2++OH-=CaCO3↓+H2O
D.氢氧化铁沉淀可被氢溴酸溶解:2Fe(OH)3+6H++2Br-=2Fe2++Br2+6H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
由黄铜矿(主要成分是CuFeS2) 炼制精铜的工艺流程示意图如下:
炼制精铜的工艺流程示意图如下:
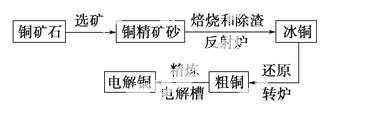
(1)在反射炉中,把铜精矿砂和石英砂混合加热到1 000 ℃左右,黄铜矿与空气反应生成Cu和Fe的低价硫化物,且部分Fe的硫化物转变为低价氧化物。该过程中两个主要反应的化学方程式分别是____________________、__________________________,反射炉内生成 炉渣的主要成分是________;
炉渣的主要成分是________;
(2)冰铜(Cu2S和FeS互相熔合而成)含Cu量为20%~50%。转炉中,将冰铜加熔剂(石英砂)在1 200 ℃左右吹入空气进行吹炼。冰铜中的Cu2S被氧化成Cu2O,生成的Cu2O与Cu2S反应,生成含Cu量约为98.5%的粗铜,该过程发生反应的化学方程式分别是____________;
(3)粗铜的电解精炼如右图所示。在粗铜的电解过程中,粗铜板应是图中电极________(填图中的字母);在电极d上发生的电极反应式为____________________________;若粗铜中还含有Au、Ag、Fe,它们在电解槽中的存在形式和位置为____________________。
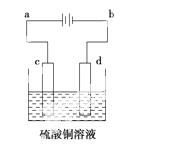
查看答案和解析>>
科目:高中化学 来源: 题型:
工业上用重铬酸钠(Na2Cr2O7)结晶后的母液(含少量杂质Fe3+)生产重铬酸钾(K2Cr2O7)。工艺流程及相关物质溶解度曲线如图
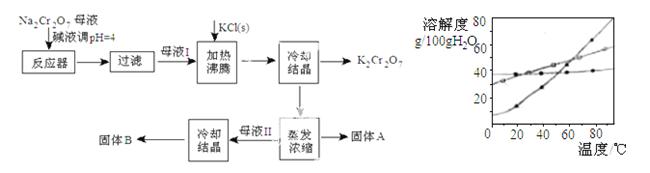 (1)由Na2Cr2O7生产K2Cr2O7的化学方程式为
(1)由Na2Cr2O7生产K2Cr2O7的化学方程式为  。通过冷过结晶析出大量K2Cr2O7的原因是 。
。通过冷过结晶析出大量K2Cr2O7的原因是 。
(2)向Na2Cr2O7母液中加碱液调pH的目的是 。
(3)固体A主要为 (填化学 式)
式) ,固体B主要为 (填化学式)。
,固体B主要为 (填化学式)。
(4)用热水洗涤固体A,回收的洗涤液转移到母液 (填“I”“II”或“III”)中,既能提高产率又可使能耗最低。
查看答案和解析>>
科目:高中化学 来源: 题型:
合成氨工业、硫酸工业的生产工艺 流程如图所示 。
。

合成塔和接触室中的反应分别为
N2(g)+3H2(g) 2NH3(g) ΔH<0;
2SO2(g)+O2(g) 2SO3(g) ΔH<0。
(1)写出流程中设备的名称:B________,X________。
(2)进入合成塔和接触室中的气体都要进行热处理,最理想的热处理方法是___________________。
(3)采用循环操作可提高原料的利用率,下列生产中,采用循环操作的是________(填序号)。
①硫酸工业 ②合成氨工业 ③硝酸工业
(4)工业上常用98.3%的浓硫酸吸收SO3而不用稀硫酸或水的原因是_______________。
(5)工业生产中常用氨-酸法进行尾气脱硫,以达到消 除污染、
除污染、 废物利用的目的。硫酸工业尾气中的SO2经处理可以得到一种化肥,该肥料的化学式是___________________。
废物利用的目的。硫酸工业尾气中的SO2经处理可以得到一种化肥,该肥料的化学式是___________________。
(6)根据化学 平衡移动原理,下列条件或措施合理的是________(填序号)。
平衡移动原理,下列条件或措施合理的是________(填序号)。
①合成氨工业在高压下进行
②合成氨工业和硫酸工业都使用催化剂
③及时将氨液化而分离
④硫酸工业中,净化后的炉气中要有过量空气
⑤合成氨工业和硫酸工业都采用适宜的温度
查看答案和解析>>
科目:高中化学 来源: 题型:
已知X、Y和Z三种元素的原子序数之和等于42。X元素原子的4p轨道上有3个未成对电子,Y元素原子的最外层2p轨道上有2个未成对电子。X跟Y可形成化合物X2Y3,Z元素可以形成负一价离子。请回答下列问题:
(1)X元素原子基态时的电子排布式为 ,该元素的符号是 。
(2)Y元素原子的电子排布图为 ,元素X与Y的电负性比较:X Y(填“>”或“<”)。
(3)X与Z可形成化合物XZ3,该化合物的空间构型为 。
(4)由元素X与镓元素组成的化合物A为第三代半导体。已知化合物A的晶胞结构如图所示。(黑球位于立方体内,白球位于立方体顶点和面心)
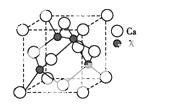
请写出化合物A的化学式 ;化合物A可由(CH3)3Ga和AsH3在700 ℃下反应制得,反应的化学方程式为 。
(5)已知(CH3)3Ga为非极性分子,则其中镓原子的杂化方式为 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com