
氰(CN)2、硫氰(SCN)2等称为拟卤素,它们与卤素单质性质相似,它们的阴离子也与卤素阴离子性质相似。例如:
2Fe+3(SCN)2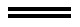 2Fe(SCN)3
2Fe(SCN)3
Ag++CN-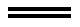 AgCN↓(白)
AgCN↓(白)
拟卤素形成的无氧酸和含氧酸一般比氢卤酸和次卤酸弱。下列反应中,不正确的是( C )
A. 2CN-+Cl2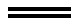 2Cl-+(CN)2
2Cl-+(CN)2
B. (CN)2+2OH-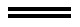 CN-+CNO-+H2O
CN-+CNO-+H2O
C. (CN)2+H2O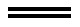 2H++CN-+CNO-
2H++CN-+CNO-
B. MnO2+4HSCN (SCN)2+Mn(SCN)2+2H2O
(SCN)2+Mn(SCN)2+2H2O
【解析】 从题中信息可以看出,拟卤素形成的无氧酸和含氧酸均为弱酸,书写离子方程式时不能拆开成离子。
 巧学巧练系列答案
巧学巧练系列答案 课课练江苏系列答案
课课练江苏系列答案科目:高中化学 来源: 题型:
请回答下列问题:
(1)写出(OCN)2的名称_______________。
(2)(CN)2中每一个原子最外层都能满足8电子稳定结构,写出(CN)2的电子式_______________。
(3)写出常温下(SCN)2和KOH溶液反应的化学方程式:_______________。
(4)已知以下四种阴离子的还原性强弱为:Br-<CN-<SCN-<I-。
写出在NaBr和KSCN的混合溶液中加入少量(CN)2反应的离子方程式_______________;写出用石墨电极电解NaCN水溶液的离子方程式_______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
氰(CN)2和硫氰(SCN)2的化学性质和卤素很相似,化学上称为“拟卤素”。它们的阴离子还原性强弱为:Cl-<Br-<CN-<SCN-<I-。试写出:
(1)(CN)2与KOH溶液反应的化学方程式:________________________。
(2)KBr和KSCN的混合溶液中加入(CN)2反应的离子方程式:________________________。
(3)硫氰酸(化学式为HSCN)有两种同分异构体。目前游离酸中的这两种互变异构体尚无法分离,硫氰酸易溶于水,其水溶液有强酸性。已知:硫氰酸中的碳、氮、硫原子在一条直线上,H、S、C、N的化合价分别为+1、-2、+4、-3,则硫氰酸的可能的结构式为_____________或__________________。
(4)硫氰酸可由硫氰酸钾与硫酸氢钾在一定条件下加热制得,这一事实说明______________
_______________________。
查看答案和解析>>
科目:高中化学 来源:2015届广东省高一第一学期期末考试化学试卷B(解析版) 题型:填空题
多原子分子氰(CN)2、硫氰(SCN)2和(OCN)2的性质与卤素单质(Cl2、Br2等)相似,故称它们为拟卤素。它们可以生成酸和盐(见下表,表中X代表F、Cl、Br或I)。
|
|
卤素 |
氰 |
硫氰 |
① |
|
“单质” |
X2[ |
(CN)2 |
(SCN)2 |
(OCN)2 |
|
酸 |
HX |
HCN |
② |
HOCN |
|
盐 |
KX |
KCN |
KSCN |
KOCN |
(1)在表中①②空格处应分别填写_______、_______。
(2)①(CN)2和KOH溶液反应的化学方程式为:__________________________。
②已知阴离子的还原性强弱为:Cl-<Br-<CN-<SCN-<I-。试写出在NaBr和KSCN的混合溶液中加入(CN)2反应的离子方程式:____________________________________。
查看答案和解析>>
科目:高中化学 来源:2014届吉林省高一下学期期中考试化学试卷(解析版) 题型:填空题
(4分) 氰[(CN)2]、硫氰[ (SCN)2]的化学性质和卤素很相似,化学上称为拟卤素.如: (SCN)2 + H2O = HSCN + HSCNO, 它们的阴离子的还原性强弱顺序为 Cl-< Br- < CN- < SCN- < I- ,试写出:
(1)(CN)2 与KOH溶液反应的化学方程式 ______________________
(2)NaBr和KSCN的混合溶液中加入(CN)2, 反应的离子方程式___________________
查看答案和解析>>
科目:高中化学 来源:江苏省2010-2011学年高三化学一轮过关测试(9) 题型:填空题
(6分)氰(CN)2、硫氰(SCN)2的化学性质和卤素(X2)很相似,化学上称为拟卤素。它们阴离子的还原性强弱为Cl-<Br-<CN-<SCN-<I-。试写出
①(CN)2与KOH溶液反应的化学方程式:
_________________________________________________________________;
②在NaBr和KSCN的混合溶液中加入(CN)2,反应的离子方程式:
_____________________________________________________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com