
| A. | pH=6的降雨是酸雨 | |
| B. | 氯气泄漏后应顺风向低处跑 | |
| C. | SO2和HClO都具有漂白性,两者的漂白原理相同 | |
| D. | 我国城市环境中的大气污染物主要有SO2、NO2、可吸入颗粒物等 |
分析 A.正常雨水的pH约为5.6;
B.氯气的密度比空气密度大;
C.二氧化硫与有色物质化合,HClO具有强氧化性可使有色物质褪色;
D.SO2、NO2均可导致酸雨发生,可吸入颗粒物可导致雾霾发生.
解答 解:A.正常雨水的pH约为5.6,溶解二氧化硫的雨水为酸雨,其pH<5.6,故A错误;
B.氯气的密度比空气密度大,则氯气泄漏后应逆风向高处跑,防止中毒,故B错误;
C.二氧化硫与有色物质化合,HClO具有强氧化性可使有色物质褪色,褪色原理分别与化合反应、氧化还原反应有关,故C错误;
D.SO2、NO2均可导致酸雨发生,可吸入颗粒物可导致雾霾发生,化石能源在工厂使用、汽车尾气等均排放污染物,则我国城市环境中的大气污染物主要有SO2、NO2、可吸入颗粒物等,故D正确;
故选D.
点评 本题考查三废处理及环境保护,为高频考点,把握常见的环境污染物、环境问题为解答关键,侧重分析与应用能力的考查,注意化学与环境的联系,题目难度不大.


科目:高中化学 来源: 题型:选择题
| A. | Fe3+、H+、SO42-、ClO- | B. | Fe3+、Fe2+、SO42-、NO3- | ||
| C. | Al3+、Na+、SO42-、CO32- | D. | K+、H+、Br-、MnO4- |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
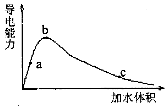 一定温度下,将一定量的冰醋酸加水稀释,稀释过程中溶液的导电性变化如图所示.则下列说法错误的是( )
一定温度下,将一定量的冰醋酸加水稀释,稀释过程中溶液的导电性变化如图所示.则下列说法错误的是( )| A. | 醋酸的电离度:c<b<a | |
| B. | 溶液的PH值:b<a<c | |
| C. | 蘸取a点溶液滴在湿润的PH试纸上,测得PH值一定偏大 | |
| D. | 若分别取a、b、c三点的溶液各10mL,各用同浓度的氢氧化钠溶液中和,消耗NaOH溶液的体积a=b=c |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | BaSO4(s)+4C(s)═BaS(s)+4CO(g)室温下不能自发进行,说明该反应的△H<0 | |
| B. | 为处理锅炉水垢中的CaSO4,可先用饱和Na2CO3溶液浸泡,再加入盐酸溶解 | |
| C. | 己知NaOH(aq)+HCl(aq)=NaCl(aq)+H2O(l)△H=-57.3kJ•mol-1,则水电离的热化学方程式为:H2O(l)?H+ (aq)+OH-(aq)△H=+57.3 kJ•mol-1 | |
| D. | 向0.1mol/L的CH3COONa溶液中加入少量醋酸钠固体,c(CH3COO-)/c(Na+ )变大 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 三氯蔗糖(C12H19Cl3O8)属于天然的糖类甜味剂 | |
| B. | 未成熟的青苹果肉遇碘酒变蓝色,成熟苹果的汁能发生银镜反应 | |
| C. | 利用盐析的方法可以用来分离、提纯蛋白质 | |
| D. | 酚醛树脂、合成橡胶、有机玻璃都属于有机高分子化合物 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | PH=7的溶液 | |
| B. | 非电解质溶于水得到的溶液 | |
| C. | 由强酸和强碱等物质的量反应得到的物质 | |
| D. | c (H+)=c (OH-) |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
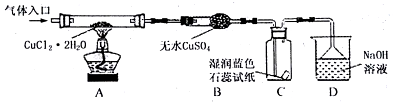
| 资料一 | CuCl2•2H2O | 在HCl气流中加热至140℃ | 产生CuCl2 | CuCl2在受热大于300℃时 | 生成CuCl和Cl2 |
| 资料二 | CuCl2•2H2O | 直接加热 | 产生Cu2(OH)2Cl2 | Cu2(OH)2Cl2在受热到200℃时 | 产生CuO |
| 步骤 | 操作描述 |
| ① | 检验装置的气密性后加药品 |
| ② | 在“气体入口”处通干燥HCl |
| ③ | 点燃酒精灯,加热 |
| ④ | 熄灭酒精灯,冷却 |
| ⑤ | 停止通入HCl,然后通入N2 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com