
肼(H2NNH2)是一种高能燃料,有关化学反应的能量变化如图所示。已知断裂1 mol化学键所需的能量(kJ):NN为942、OO为500、NN为154,则断裂1 mol NH键所需的能量(kJ)是( )

A.194 B.391
C.516 D.658
科目:高中化学 来源: 题型:
某苯的同系物分子式为C11H16,经分析分子中除含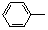 外,不再含其他环状结构,还含有3个—CH3、1个—CH2—、1个
外,不再含其他环状结构,还含有3个—CH3、1个—CH2—、1个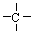 ,它可能的结构有( )
,它可能的结构有( )
A. 1种 B.2种 C.3种 D. 4种
查看答案和解析>>
科目:高中化学 来源: 题型:
以NA代表阿伏加德罗常数,且已知C2H2(g)+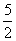 O2(g)===2CO2(g)+H2O(l) ΔH=-1 300 kJ/mol,则下列说法中正确的是( )
O2(g)===2CO2(g)+H2O(l) ΔH=-1 300 kJ/mol,则下列说法中正确的是( )
A.当有20NA个电子转移时,热化学方程式为2C2H2(g)+5O2(g)===4CO2(g)+2H2O(l) ΔH=-2 600 kJ/mol
B.当有4NA个碳氧共有电子对生成时,放出1 300 kJ的能量
C.若生成NA个水蒸气分子的焓变为ΔH ′,则ΔH′<ΔH
D.题给反应为吸热反应
查看答案和解析>>
科目:高中化学 来源: 题型:
如图是以铅蓄电池为电源,模拟氯碱工业电解饱和食盐水的装置图(C、D均为石墨电极)。
已知:铅蓄电池在放电时发生下列电极反应:
负极Pb+SO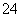 -2e-===PbSO4
-2e-===PbSO4
正极PbO2+4H++SO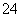 +2e-===PbSO4+2H2O
+2e-===PbSO4+2H2O
(1)请写出电解饱和食盐水的化学方程式
_____________________。
(2)若在电解池中C极一侧滴酚酞试液,电解一段时间后未呈红色,说明铅蓄电池的A极为________极。
(3)用铅蓄电池电解1L饱和食盐水(食盐水足量、密度为1. 15 g/cm3)时,
①若收集到11.2L(标准状况下)氯气,则至少转移电子________mol。
②若铅蓄电池消耗H2SO42 mol,则可收集到H2的体积(标准状况下)为________L。
③若消耗硫酸a mol,电解后除去隔膜,所得溶液中NaOH的质量分数表达式为(假设氯气全部排出)________(用含a的代数式表示)。
查看答案和解析>>
科目:高中化学 来源: 题型:
常温下,在pH都是9的NaOH和CH3COONa两种溶液中,设由水电离产生的c(OH-)分别为a mol·L-1与b mol·L-1,则a与b的关系为( )
A.a>b B.a=10-4b
C.b=10-4a D.a=b
查看答案和解析>>
科目:高中化学 来源: 题型:
25 ℃时有甲、乙两杯醋酸溶液,甲的pH=2,乙的pH=3,下列判断正确的是( )
A.甲中由水电离出来的H+的物质的量浓度是乙中由水电离出来的H+的物质的量浓度的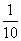
B.甲、乙两杯溶液的物质的量浓度之间的关系为c(甲)=10c(乙)
C.中和等物质的量的NaOH,需甲、乙两杯醋酸的体积(V)之间的关系为10V(甲)>V(乙)
D.甲中的c(OH-)为乙中的c(OH-)的10倍
查看答案和解析>>
科目:高中化学 来源: 题型:
甲烷自热重整是先进的制氢方法,包含甲烷氧化和蒸汽重整。向反应系统同时通入甲烷、氧气和水蒸气,发生的主要化学反应有:
| 化学方程 | 焓变ΔH/kJ·mol-1 | 活化能Ea/kJ·mol-1 | |
| 甲 烷 氧 化 | CH4(g)+2O2(g)=== CO2(g)+2H2O(g) | -802.6 | 125.6 |
| CH4(g)+O2(g)=== CO2(g)+2H2(g) | -322.0 | 172.5 | |
| 蒸 汽 重 整 | CH4(g)+H2O(g)=== CO(g)+3H2(g) | +206.2 | 240.1 |
| CH4(g)+2H2O(g)=== CO2(g)+4H2(g) | +165.0 | 243.9 |
回答下列问题:
(1)反应CO(g)+H2O(g)===CO2(g)+H2(g)的ΔH=________kJ·mol-1。
(2)在初始阶段,甲烷蒸汽重整的反应速率________甲烷氧化的反应速率(填“大于”“小于”或“等于”)。
(3)对于气相反应,用某组分(B)的平衡压强(pB)代替物质的量浓度(cB)也可表示平衡常数(记作Kp),则反应CH4(g)+H2O(g)CO(g)+3H2(g)的Kp=________,随着温度的升高,该平衡常数________(填“增大”“减小”或“不变”)。
(4)从能量角度分析,甲烷自热重整方法的先进之处在于
___________________________________________________________________。
(5)在某一给定进料比的情况下,温度、压强对H2和CO物质的量分数的影响如下图:
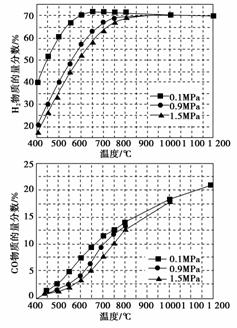
①若要达到H2物质的量分数>65%、CO物质的量分数<10%,以下条件中最合适的是________。
A.600 ℃,0.9 MPa B.700 ℃,0.9 MPa
C.800 ℃,1.5 MPa D.1 000 ℃,1.5 MPa
②画出600 ℃,0.1 MPa条件下,系统中H2物质的量分数随反应时间(从常温进料开始计时)的变化趋势示意图:
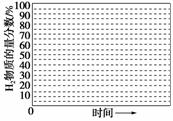
(6)如果进料中氧气量过大,最终导致H2物质的量分数降低,原因是
___________________________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
美国麻省理工学院的丹尼尔·诺切拉博士公布了自己团队研发的“人造树叶”,它可以与燃料电池共同构成一个新的发电装置——太阳能燃料电池,工作原理如图所示,下列有关叙述正确的是( )
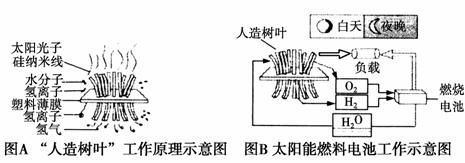
A.“人造树叶”上发生的反应为6CO2+6H2O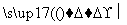 C6H12O6+6O2
C6H12O6+6O2
B.图A中塑料薄膜上部的反应为2H++2e-===H2↑
C.图B燃料电池工作时的负极反应物为O2
D.太阳能燃料电池的优点为无论天气如何,均能持续供应电能,并且实现对环境的“零排放”
查看答案和解析>>
科目:高中化学 来源: 题型:
下列说法错误的是( )
A.NH4NO3溶于水吸热,说明其溶于水不是自发过程
B.同一种物质气态熵值最大,液态时次之,而固态时熵值最小
C.借助于外力能自发进行的过程,其体系的能量趋向于从高能状态转变为低能状态
D.由焓判据和熵判据组合而成的复合判据,更适合于所有的过程
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com