
| A. | “测定气体摩尔体积”实验中,若温度高于0℃,气体摩尔体积一定大于22.4L/mol | |
| B. | “浓硫酸稀释”实验中,将水慢慢注入浓硫酸中,并不断搅拌 | |
| C. | “实验室制取氢气”实验中,收集装置与氯化氢气体的收集装置相同 | |
| D. | “萃取”实验中,振荡后,需要打开分液漏斗活塞,使漏斗内气体放出 |
分析 A.温度和压强都影响气体摩尔体积;
B.稀释浓硫酸时,应该将浓硫酸加入水中,
C.氢气的密度小于氯化氢,收集氢气应该采用向下排空气法收集;
D.振荡后分液漏斗中气压增大,若不放气可能会发生危险.
解答 解:A.影响气体摩尔体积的因素有温度、压强,温度高于0℃时,压强不确定,气体摩尔体积可能大于、等于或小于22.4L/mol,故A错误;
B.“浓硫酸稀释”实验中,浓硫酸的密度大于水,且放出大量热,应该将浓硫酸慢慢注入水中,并不断搅拌,故B错误;
C.“实验室制取氢气”实验中,收集氢气应该采用排水法后向下排空气法,而收集氯化氢气体采用向上排空气法,二者的收集装置不同,故C错误;
D.萃取”实验中,振荡后,打开活塞使漏斗内气体放出以防止分液漏斗内压强过大引起危险,该操作方法合理,故D正确;
故选D.
点评 本题考查了化学实验方案的评价,题目难度不大,涉及浓硫酸稀释、氢气制取与收集、萃取操作方法等知识,明确化学实验基本操作方法为解答关键,试题培养了学生的分析能力及化学实验能力.


 中考解读考点精练系列答案
中考解读考点精练系列答案 各地期末复习特训卷系列答案
各地期末复习特训卷系列答案科目:高中化学 来源: 题型:多选题
| 元素 | 甲 | 乙 | 丙 | 丁 | 戊 |
| 化合价 | -4 | +1 | -4 | -2 | -1 |
| A. | 乙的常见氧化物有两种 | |
| B. | 气态氢化物稳定性:丙<丁 | |
| C. | 丙的氧化物能与戊的氢化物的水溶液反应 | |
| D. | 原子半径大小:甲>丙 |
查看答案和解析>>
科目:高中化学 来源: 题型:计算题
查看答案和解析>>
科目:高中化学 来源: 题型:计算题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 医用消毒酒精是一种有机化合物 | |
| B. | 有沉淀生成的过程一定发生了化学变化 | |
| C. | 金属钠属于遇湿易燃危险化学品 | |
| D. | 泡沫灭火器中药剂为干冰和起泡剂 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
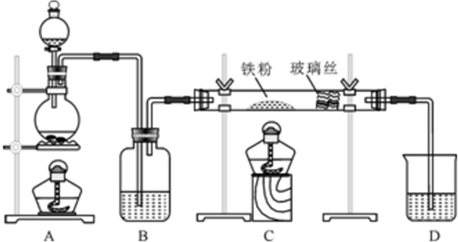
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 用乙醇和浓硫酸制乙烯 | B. | 用电解水获得的氢气来合成氨 | ||
| C. | 用晒盐后的卤水制溴单质 | D. | 用氢氧化钠和二氧化碳制碳酸钠 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Fe$\stackrel{稀H_{2}SO_{4}}{→}$FeSO4(aq)$\stackrel{NaOH(aq)}{→}$Fe(OH)2 | |
| B. | Al3+$\stackrel{过量氨水}{→}$Al${\;}_{2}^{-}$$\stackrel{CO_{2}}{→}$Al(OH)3 | |
| C. | NH3$\stackrel{O_{2}}{→}$NO$\stackrel{H_{2}O}{→}$HNO3 | |
| D. | 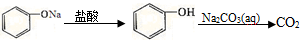 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com