
�����й�ʵ�������ԭ����ȷ����
A���õ�������ʱ��Ҫ������ȡ������С��������������ʣ����Ʋ��ܷŻ�ԭ�Լ�ƿ��
B������ˮ��pH�����ò�����պȡ��ˮ����pH��ֽ�ϣ������ɫ��ͱ���ɫ���Ƚ�
C���Ƚϲ�ͬŨ��������Na2S2O3��Ӧ�����ʲ���ͨ���۲������ݳ������Ƚϣ���ΪSO2������ˮ
D��ͨ���ⶨ�����ʵ���Ũ�ȵ�NaCl��Na2S��Һ��pH���Ƚ���������Ԫ�صķǽ�����ǿ��

| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ��2016�����ʡ����9���¿��Ի�ѧ�Ծ��������棩 ���ͣ�ѡ����
��ѧ��ѧ��Ҫ������ѧר�������������������йػ�ѧ������ȷ����
A��CO2�ĵ���ʽ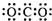
B��Cl���Ľṹʾ��ͼ��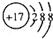
C����ϩ�Ľṹ��ʽC2H4
D��Z������Ϊ37����ԭ��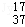 Cl
Cl
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2015-2016ѧ��ӱ�������ѧ�߶���ѧ�ڵ�һ��������ѧ�Ծ��������棩 ���ͣ������
��8�֣��ݱ�����ƻ����˾������һ����Һ̬�״�Ϊԭ�ϣ���KOHΪ����ʵ������ֻ��Ŀɳ��ĸ�Чȼ�ϵ�أ���һ�ε������ʹ��һ���£���ͼ��һ���绯ѧ���̵�ʾ��ͼ��

��֪�׳ص��ܷ�ӦʽΪ��2CH3OH��3O2��4KOH K2CO3��6H2O ����գ�
K2CO3��6H2O ����գ�
��1�����ʱ����ԭ��صĸ������Դ______������,�������ĵ缫��ӦΪ________��
��2���ڴ˹���������ȫ��Ӧ���ҳ���B������������648g����׳�������������O2____L����״���£���
��3������Ʊ�Al(OH)3ʱ���缫�ֱ�ΪAlƬ��ʯī������ܷ�Ӧ����ʽΪ ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2015-2016ѧ��ӱ������ص�һ��ѧ�߶���ѧ�ڵ�һ���¿��Ի�ѧ�Ծ��������棩 ���ͣ�ѡ����
��֪��Fe2O3(s) +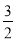 C(s)=
C(s)=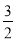 CO2(g) +2Fe(s) ��H1=+234.1 kJ��mol-1,C(s)+ O2(g)=CO2(g) ����2=-393.5 kJ��mol-1,��2Fe(s) +
CO2(g) +2Fe(s) ��H1=+234.1 kJ��mol-1,C(s)+ O2(g)=CO2(g) ����2=-393.5 kJ��mol-1,��2Fe(s) +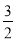 O2(g) =Fe2O3(s) �Ħ�H��
O2(g) =Fe2O3(s) �Ħ�H��
A��-824.4 kJ��mol-1
B��-627.6 kJ��mol-1
C��-744.7 kJ��mol-1
D��-169.4 kJ��mol-1
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2016���㽭ʡ������ѧ�ڵ�һ��ģ�⿼�Ի�ѧ�Ծ��������棩 ���ͣ������
��6�֣���ˮ���ܶ�����ˮ���п��ٵ�ɱ��������ҩ��ͨ�����������㡣�������Ⱦ�[Cl2Na(NCO)3����Ԫ��Ϊ+1��]����ˮ��Ӧ�����ɴ����ᣨHClO����ɱ���������ã������Ӻ��ڲ���������ƣ�Na2SO3���ܳ����ɽ�ˮ�е����ȣ������ᣩ��ȥ��
��1�����Ⱦ��е�Ԫ�صĻ��ϼ�Ϊ ��
��2���������ƽ�ˮ�ж���������ȥ�����ӷ�Ӧ����ʽΪ ��
��3������������Һ�ڿ������ױ��ʣ���д����������������Һ�Ƿ���ʵķ��� ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2016������ʡ������ѧ�ڵ�һ���¿���ѧ�Ծ��������棩 ���ͣ�ѡ����
��֪NH3��HCl��������������Ȫʵ������塣����ͬ��ͬѹ���õ������ƿһ���ռ���NH3����һ���ռ�HCl��N2�Ļ�����壬��ͼ��ʾ����Ȫʵ��ֹͣ��������ƿ����Һ�Ĺ�ϵ��(��������ƿ�����ʵ���ɢ����ˮ�����ʰ�NH3����)
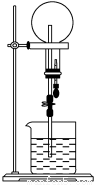
A�����ʵ����ʵ���Ũ����ͬ�����ʵ�����������ͬ
B�����ʵ�����������ͬ�����ʵ����ʵ���Ũ�Ȳ�ͬ
C�����ʵ����ʵ���Ũ�Ⱥ����ʵ�������������ͬ
D�����ʵ����ʵ���Ũ�Ⱥ����ʵ�������������ͬ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2016��ȫ���Ƽ�����������������ѧ�Ծ��������棩 ���ͣ�ѡ����
���з�Ӧ�����ӷ���ʽ����ȷ����
A��Na2O2��ˮ��Ӧ��Na2O2 + H2O = 2Na+ + 2OH- + H2��
B��FeSO4��Һ��H2O2��Һ��ϣ�Fe2++H2O2+2H+�TFe3++2H2O
C����Na2SiO3��Һ��ͨ�������SO2��SiO3 2- +SO2 +H2O = SO3 2- +H2SiO3��
D��NH4 HCO3ϡ��Һ�������Ca(OH)2��Һ��ϣ�NH4++HCO3-+2OH-+Ca2+�TCaCO3��+H2O+NH3��H2O
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2015-2016ѧ��ɽ����Ȫʮ���и�����һ�νο��Ի�ѧ�Ծ��������棩 ���ͣ�ʵ����
��11�֣���Na+Ũ��Ϊ0.9mol/L��ij������Һ�У������ܺ����±��е����������ӣ�
������ | K+��Ag+��Mg2+��Ba2+ |
������ | NO3-��CO32-��SiO32-��SO42- |
ȡ����Һ100mL��������ʵ�飨��������ڱ�״���²ⶨ����
��� | ʵ������ | ʵ���� |
�� | �����Һ�м�������ϡHCl | ������ɫ�������ų�1.12L���� |
�� | ����ķ�Ӧ���Һ���ˣ��Գ���ϴ�ӡ����������أ��������ù������� | ��������Ϊ3.6g |
�� | �ڢ����Һ�еμ�BaC12��Һ | ���������� |
�Իش��������⣺
��1��ʵ��I��ȷ��һ�������ڵ������� ��
��2��ʵ��I�����ɳ��������ӷ���ʽΪ ��
��3��ͨ��ʵ��I����ͱ�Ҫ���㣬��д�±��������ӵ�Ũ�ȣ��ܼ�����ģ���д��������һ�������ڵ������0��������ȷ���Ƿ���ڵ������������
������ | NO3- | CO32- | SiO32- | SO42- |
c/mol��L-1 |
��4���ж�K+�Ƿ���� ��������������СŨ�ȣ���������˵������ ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2016�����һ�и������¿���ѧ�Ծ��������棩 ���ͣ�ѡ����
�о�����CuSO4��FeS2��һ�������¿ɷ������·�Ӧ�� 14CuSO4+5FeS2+12H2O =7Cu2S +5FeSO4 +12H2SO4������˵����ȷ����
A��FeS2�е���Ԫ��ȫ��������
B��5 mol FeS2������Ӧ����10 mol����ת��
C��������SO42-��һ��������������
D��FeS2ֻ������ԭ��
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com