
| A. | Na2CO3溶液 | B. | 溴水 | C. | 新制Cu(OH)2 | D. | 福尔马林 |
分析 根据物质的性质进行鉴别,苯酚能与溴水反应生成三溴苯酚,己烯含有C=C官能团,与溴水发生加成反应,碘化钾可与溴水发生氧化还原反应,苯不溶于水,乙酸溶于水.
解答 解:A.碳酸钠溶液不能区分碘化钾溶液和苯酚溶液,也不能区分苯和己烯,故A错误;
B.碘化钾可与溴水发生氧化还原反应,溶液变为紫色或红褐色,苯酚能与溴水反应生成三溴苯酚沉淀,乙酸和溴水形成的溶液不分层,己烯含有C=C官能团,苯不溶于水,加入溴水,上层呈橙色,与溴水发生加成反应而使溴水褪色,现象各不同,故B正确;
C.新制Cu(OH)2只能鉴别出乙酸,不能区分碘化钾溶液、苯酚溶液,也不能区分苯和己烯,故C错误;
D.福尔马林中含有甲醛,甲醛除了催化剂加热条件下与苯酚发生反应生成酚醛树脂之外,与其他几种物质都不反应,故D错误;
故选B.
点评 本题考查有机物的鉴别,题目难度不大,本题注意常见有机物的性质,在鉴别有机物时,不要忽略有机物的物理性质.


科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
 ,乙为
,乙为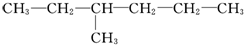 .下列有关它们命名的说法正确的是( )
.下列有关它们命名的说法正确的是( )| A. | 甲、乙的主链碳原子数都是6个 | B. | 甲、乙的主链碳原子数都是5个 | ||
| C. | 甲的名称为2-丙基-1-丁烯 | D. | 乙的名称为3-甲基己烷 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 铁和盐酸反应 2Fe+6H+═2Fe3++3H2↑ | |
| B. | 小苏打溶液与少量澄清石灰水混合:Ca2++OH-+HCO3-═CaCO3↓+H2O | |
| C. | AlCl3溶液中加入足量的氨水:Al3++3OH-═Al(OH)3↓ | |
| D. | Na2CO3溶液中通入少量CO2:CO32-+CO2+H2O═2HCO3- |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com