
| A.用导线将铁片和铜片连接后,放入一盛有稀 H2SO4溶液的烧杯中 |
| B.Cu片作阳极,铁片作阴极,电解一定量的H2SO4溶液 |
| C.Cu片作阴极,铁片作阳极,电解一定量的H2SO4溶液 |
| D.将铁片直接放入一盛有稀 H2SO4溶液的烧杯中 |
科目:高中化学 来源:不详 题型:单选题

| A.盐桥中的Cl-向乙烧杯方向移动 | B.盐桥中有电子通过 |
| C.乙中的铜棒逐渐变细 | D.片刻后可观察到滤纸a点变红色 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.温度越高,金属腐蚀速率越快 |
| B.在铁管外壁上镀锌可防止其被腐蚀 |
| C.金属被腐蚀的本质是金属发生了氧化反应 |
| D.将钢闸门与直流电源的正极相连可防止其被腐蚀 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
 Fe(OH)2 + Ni(OH)2。
Fe(OH)2 + Ni(OH)2。| A.NiO2 | B.Fe | C.Fe(OH)2 | D.Ni(OH)2 |
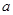 g M,则金属M的相对原子质量为 (用含“
g M,则金属M的相对原子质量为 (用含“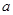 、x”的表达式表示)。
、x”的表达式表示)。 查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
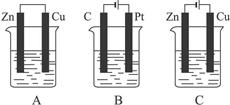
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
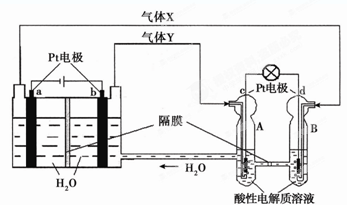
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
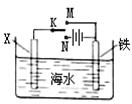
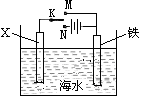
| A.X为锌棒,K置于M,可减缓铁的腐蚀,铁电极上发生的反应为2H++2e-=H2↑ |
| B.X为锌棒,K置于M,外电路电流方向是从X到铁 |
| C.X为碳棒,K置于N,可减缓铁的腐蚀,利用的是外加电流的阴极保护法 |
| D.X为碳棒,K置于N,在X电极周围首先失电子的是Cl- |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com