
| A. | 19gNHD2和19gNH2T中含有的中子数均为10NA | |
| B. | 标准状况下,22.4LO2参加反应转移的电子数一定是4NA | |
| C. | 1molCnH2n中含有的共用电子对数为(3n+1)NA | |
| D. | 2molSO2和1molO2在一定条件下充分反应后,所得混合气体的分子数大于2NA |
分析 A.19gNHD2物质的量=$\frac{19g}{19g/mol}$=1mol,19gNH2T物质的量=$\frac{19g}{19g/mol}$=1mol,中子数=质量数-质子数计算;
B.标准状况下气体物质的量n=$\frac{22.4L}{22.4L/mol}$=1mol,氧气参加反应变化为-2价,也可以变化为-1价;
C.分子式为CnH2n分子中含有n个C-C键,2n个C-H键;
D.二氧化硫和氧气反应生成三氧化硫是可逆反应不能进行彻底.
解答 解:A.中子数=质量数-质子数计算,NHD2和NH2T中,19gNHD2物质的量=$\frac{19g}{19g/mol}$=1mol,中子数=14-7+1-1+(2-1)×2=9,19gNH2T物质的量=$\frac{19g}{19g/mol}$=1mol,中子数=14-7+(1-1)×2+3-1=9,19gNHD2和19gNH2T中含有的中子数均为9NA,故A错误;
B.标准状况下气体物质的量n=$\frac{22.4L}{22.4L/mol}$=1mol,氧气参加反应变化为-2价,也可以变化为-1价,如钠和氧气反应生成氧化钠,1mol氧气反应电子转移4mol,钠和氧气加热反应生成过氧化钠1mol氧气反应电子转移2mol,故B错误;
C.1molCnH2n中含有的共用电子对数为3nNA ,故C错误;
D.二氧化硫和氧气反应生成三氧化硫是可逆反应不能进行彻底,1mol O2和2mol SO2在一定条件下,充分反应生成SO3的分子数小于2NA ,所得混合气体的分子数大于2NA ,故D正确;
故选D.
点评 本题考查了阿伏伽德罗常数的分析应用,主要是气体摩尔体积条件应用、可逆反应分析、氧化还原反应的转移计算应用、分子结构,掌握基础是关键,题目难度中等.


 期末冲刺100分创新金卷完全试卷系列答案
期末冲刺100分创新金卷完全试卷系列答案科目:高中化学 来源: 题型:解答题
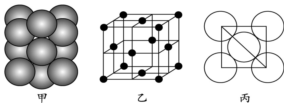 已知 X、Y、Z、Q、R、E六种前四周期元素中,原子序数X<Y<Z<Q<R<E,其结构或性质信息如表.
已知 X、Y、Z、Q、R、E六种前四周期元素中,原子序数X<Y<Z<Q<R<E,其结构或性质信息如表.| 元素 | 结构或性质信息 |
| X | 原子的L层上s电子数等于p电子数 |
| Y | 原子核外的L层有3个未成对电子 |
| Z | 地壳中含量最多的元素 |
| Q | 单质常温常压下是气体,原子的M层上有1个未成对的p电子 |
| R | 核电荷数是Y与Q的核电荷数之和 |
| E | N能层上只有一个电子,K、L、M层均排满电子 |
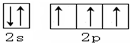 .X的一种氢化物相对分子质量为26,其分子中的σ键与π键的键数之比为3:2.
.X的一种氢化物相对分子质量为26,其分子中的σ键与π键的键数之比为3:2.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 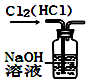 用图所示装置除去Cl2中的HCl | |
| B. | 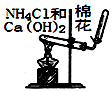 用图所示装置实验室制NH3 | |
| C. | 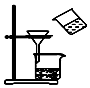 用图所示装置分离MnO2和KCl | |
| D. | 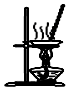 用图所示装置蒸干NH4Cl饱和溶液制备NH4Cl晶体 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
| 有机物 | 试剂 | 现象 |
| (1)甲苯 | a.碘水 | A.出现光亮的银镜 |
| (2)乙醛 | b.高锰酸钾酸性溶液 | B.呈紫色 |
| (3)苯酚 | c.浓硝酸 | C.呈蓝色 |
| (4)淀粉 | d.新制银氨溶液 | D.呈黄色 |
| (5)蛋白质 | e.三氯化铁溶液 | E.紫色褪去 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ②④ | B. | ①③⑤⑦ | C. | ④⑧ | D. | ②④⑥⑧ |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| 选项 | 实验操作 | 实验目的或结论 |
| A | 将Al2(SO4)2、NaOH溶液相互滴加 | 鉴别Al2(SO4)3、NaOH溶液 |
| B | 向某溶液中滴加氯水,再滴加KSCN溶液,溶液变成红色 | 该溶液中一定含有Fe2+ |
| C | 向NaHS溶液中滴入酚酞,溶液变红色 | HS-水解程度大于电离程度 |
| D | 向蛋白质溶液中加入CuCl2或(NH4)2SO4饱和溶液,均有沉淀 | 蛋白质均发生了变性 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 氯气具有酸性,可与烧碱或石灰乳反应制备含氯消毒剂 | |
| B. | 明矾在水中能形成胶体,可作为净水剂 | |
| C. | 氢氟酸具有弱酸性,可用氢氟酸雕刻玻璃 | |
| D. | 过氧化钠具有强氧化性,可用作潜水艇中氧气的来源 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com